Melanomani davolashda MRNK vaktsinalarining evolyutsiyasi va taraqqiyoti: kelajak istiqbollari
Aug 08, 2023
Abstrakt: o'simta antijenlarini kodlovchi mRNK vaktsinalari saraton hujayralariga qarshi xostning immun tizimini sezgirlashtirib, antigen taqdimotini va immun javobini kuchaytirishi mumkin. COVID-19 pandemiyasi boshlanganidan beri mRNK vaktsinalariga qiziqish ortib bormoqda, chunki virusga qarshi emlash kasallik tarqalishini cheklash chorasi sifatida xizmat qilgan. So'nggi bir necha o'n yilliklarda immunoterapiya melanomani davolashning asosi bo'lganligini hisobga olsak, maqsadli mRNK vaktsinalari orqali tug'ma immunitetni yanada oshirish melanomani davolashda keyingi muhim yutuq bo'lishi mumkin. Sichqoncha saratoni modellaridan olingan klinikagacha bo'lgan ma'lumotlar allaqachon mRNK vaktsinalarining saraton kasalligiga qarshi immunitet reaktsiyalarini qo'zg'atish qobiliyatini isbotlagan. Bundan tashqari, mRNK vaktsinalarini olgan melanomali bemorlarda o'ziga xos immun javoblar kuzatilgan, yaqinda o'tkazilgan KEYNOTE{1}} sinovi esa mRNK-4157/V940 vaktsinasini immun bilan birgalikda melanoma davolash algoritmiga kiritishni aniqlashi mumkin. nazorat nuqtasini inhibe qilish. Mavjud ma'lumotlar qo'shimcha sinovdan o'tkazilib, ko'rib chiqilgach, tadqiqotchilar saratonni davolashning istiqbolli yo'li haqida allaqachon ishtiyoq qozonmoqda.
Kalit so'zlar: mRNK; vaksinalar; melanoma; saraton; immunoterapiya

cistanche qo'shimchasining foydalari - Antitumor
1.Kirish
mRNK kashf etilgan va ajralmas va kuchli gen transkripsiyasi vositachisi [1] sifatida e'tirof etilganidan beri, hujayra madaniyati va sichqon modellarida sun'iy ravishda oqsil ifodasini induktsiya qilish saraton tadqiqotlarida keng qo'llanildi [2-4]. 1990–2000 yillar davomida mRNK asosidagi saratonga qarshi vaktsinani ishlab chiqish bo'yicha bir nechta urinishlar karsinoembrionik antigen (CEA) va glikoprotein 100 (gp100) kabi aniqlangan saraton antijenlarining induktsiyasi yordamida klinikdan oldingi darajada amalga oshirildi. [5–7]. Shunga qaramay, mRNK asosidagi vaktsinalar, asosan, ularning immunogen taʼsirini hamda barqarorligini taʼminlash uchun tegishli ilmiy va texnik vositalarning yoʻqligi sababli, COVID{12}} pandemiyasi avj olguncha klinik amaliyotga deyarli kiritilmagan edi [8. ,9]. So'nggi o'n yilliklar davomida mRNK vaktsinalarini ishlab chiqarish bo'yicha tajriba asta-sekin o'sib bordi va oxir-oqibat ularni yaqinda pandemiyadan himoya qilishning asosiy bosqichiga aylanish imkonini berdi [8,9]. Haqiqatan ham, 2020–2021 yillar davomida Pfifizer va Moderna mRNK vaktsinalari klinik sinovlarda oʻrganilib, rasman tasdiqlangan va virus tarqalishini cheklash va infektsiyalanganlarda uning klinik koʻrinishlarining zoʻravonligini kamaytirish maqsadida jamoatchilikka qoʻllanilgan. shaxslar [10–12]. Shu nuqtai nazardan, antineoplastik davolash sifatida mRNK vaktsinalariga ilmiy qiziqish qayta tiklandi. mRNK vaktsinalari antigen taqdimotida vositachilik qiladi, chunki ular dendritik hujayralar tomonidan kiritilgan, natijada ular yuzasida vaktsina bilan kodlangan saraton antijenlarini ifodalaydi va shu bilan sitotoksik CD8 plus, shuningdek, yordamchi CD4 plyus hujayra faollashuvini keltirib chiqaradi, shu bilan birga yallig'lanish vositachilarining chiqarilishini oshiradi [13] . Demak, ular DNKning yadroviy tuzilishiga aralashmasdan yoki hujayra oqsilining ifodalanishiga doimiy ta'sir qilmasdan immun hujayralarga genetik ma'lumotni etkazib berishning istiqbolli usuli hisoblanadi, chunki mRNK xavfli mutatsiyalarni keltirib chiqarishi mumkin bo'lgan hujayra yadrosiga kira olmaydi [8,9,14]. ,15]. Bundan tashqari, mRNK virusli yoki plazmid vektorlarisiz uzatilishi mumkin, tabiiy ravishda xost hujayrasi tomonidan eritiladi va ishlab chiqarish DNK bilan bog'liq terapevtiklarga qaraganda arzonroq bo'lib, yanada xavfsizroq ma'muriyat va keng ko'lamli ishlab chiqarish imkonini beradi [8,9,13, 16,17]. mRNK vaktsinalari ex vivo qo'llanilishi mumkin; antigen taqdim qiluvchi hujayralar (masalan, dendritik hujayralar) bemordan ajratiladi, mRNK bilan kodlangan antijenlarning ekspressiyasini qo'zg'atish uchun mRNK vaktsinasi bilan inkubatsiya qilinadi va nihoyat xostga qayta kiritiladi. Muqobil yondashuv bemorga mRNK vaktsinasini to'g'ridan-to'g'ri yuborishdan iborat va protamin (qatronga o'xshash ishqoriy oqsil) va polietilenimin kabi polimerlar kabi stabillashtiruvchi katyonik komplekslarni birlashtirish orqali amalga oshirilishi mumkin bo'lgan xavfsiz vaktsina tuzilishini talab qiladi [8,9]. ,18]. Keyinchalik so'nggi texnologik yutuqlar mRNK vektorlari sifatida ishlatiladigan lipid nanozarrachalarini ishlab chiqishga olib keldi, mRNKni sitoplazmaga xavfsiz tashish, chunki ular ham barqaror, ham endositozga moyil bo'lib, yuklangan mRNK funktsiyasiga xalaqit bermaydi [8,9,18]. So'nggi o'n yilliklar davomida mRNK vaktsinalarini ishlab chiqarish jarayoni keng qamrovli o'rganildi va takomillashtirildi. Ishtirok etilgan mRNK molekulasining transkripsiyasi maqsadli antigenni kodlovchi DNK ketma-ketligiga asoslanib, in vitro sharoitda amalga oshiriladi, ikkinchisi chiziqli plazmidga kiritilgan [8,9,18]. Hujayradan tashqari RNazalar (mRNKni parchalovchi fermentlar) tomonidan parchalanishdan qochib, yuborilgan mRNKning bir qismi ribosoma apparati tomonidan oqsillarga aylantirilishi uchun endositoz orqali maqsadli hujayra sitoplazmasiga kiradi. Olingan oqsil hujayradan tashqariga chiqarilishi yoki tashilishi va hujayradan tashqari sirtga ta'sir qilishi mumkin, MHC (asosiy gistokompozitsiya kompleksi) sinf I yoki II oqsillari bilan biriktiriladi [8,9,18]. Yuqorida aytib o'tilganidek, mRNKning zaif tabiati va hujayradan tashqari RNazalarning mavjudligini hisobga olgan holda, barqarorlik samarali mRNK emlashning kalitidir. Kuchli mRNK vaktsinasini yaratishga kodlash maydonini o'z ichiga olgan 50 va 30 tarjima qilinmagan hududlarni kiritish orqali erishish mumkin, bu uning buzilishini oldini oladi. mRNK ketma-ketligini yanada barqarorlashtirish uchun 50 maydonini metilatsiyalash va poli(A) dumini (bir nechta adenozin monofosfatlar ketma-ketligi) 30 maydonga biriktirish orqali qo'llaniladi [8,9,18]. mRNKga asoslangan muolajalar keng ko'lamli salohiyatga ega; ular malign o'smalarga, yuqumli kasalliklarga va allergiyaga qarshi qo'llanilishi mumkin. Onkologiyada mRNKga qarshi emlashning maqsadi, qo'llash usuli yoki kodlangan ketma-ketliklardan qat'i nazar, immunitet nazoratini kuchaytirish va saraton hujayralariga qarshi immunitet tizimining faolligini kuchaytirishdir [8,9,16,18]. Onkologiya sohasida o'rganilayotgan mRNK vaktsinalari ketma-ketligi bilan kodlangan maqsadli oqsillar uchta asosiy toifadan biriga kiradi: 1. DNK o'zgarishlari, alternativ mRNK qo'shilishi yoki transkripsiyadan keyingi o'zgarishlar tufayli faqat o'simta tomonidan ifodalangan neoantigenlar yoki mutatsiyaga uchragan oqsil shakllari. Ular yuqori va o'simtaga xos immunogenlik bilan tavsiflanadi va o'simta turi bilan bog'liq bo'lishi mumkin yoki hatto bemorga xos antijenler bo'lishi mumkin [19]. 2. MAGE-A3 (MAGE oila raqami A3), NY-ESO-1 (Nyu-York qizilo'ngach skuamozi) kabi normal to'qimalarda topilishi mumkin bo'lgan o'sma bilan bog'liq antijenler hujayrali karsinoma 1), tirozinaza, TPTE (tensin homologiyasi bilan transmembran fosfataza) va gp100 [20]. 3. Yallig'lanish vositachilari, IL{80}} (interleykin-12) va GM-CSF (granulotsitlar-makrofaglar koloniyasini stimulyatsiya qiluvchi omil) kabi hujayradan tashqari chiqariladigan kimyokinlar yoki TLR4 (toll) kabi hujayra yuzasida ifodalangan -kabi retseptor 4) [21]. Yuqoridagi oqsillar va mRNK ketma-ketliklarini izolyatsiya qilish va eng immunogen neoantigenlarni tanib olish va tegishli DNK o'zgarishlari har xil turdagi mRNK vaktsinalarini ishlab chiqarishda ishlatilishi mumkin bo'lgan mos DNK shablonlarini yaratishga imkon berdi. malign o'smalar [8,9,16,18,21]. Immunitetni nazorat qilish punkti ingibitorlari - bu o'simta hujayralari tomonidan qo'zg'atilishi mumkin bo'lgan xost sitotoksik T-limfotsitlarining deaktivatsiyasini o'chirib qo'yadigan immun yoki malign hujayralar yuzasida o'ziga xos retseptorlarga qaratilgan monoklonal antikorlar. Bunday vositalar (masalan, pembrolizumab, nivolumab, ipilimumab) 2010 yildan buyon saratonni davolashda inqilob qildi, turli neoplazmalarni davolash ehtimolini oshirdi, ob'ektiv javoblarni uzoq vaqt davomida qo'zg'atdi va bemorning omon qolishini sezilarli darajada uzaytirdi [22]. Eng muhimi, immunoterapiya melanoma kabi kimyoviy sezgir bo'lmagan neoplazmalar bilan og'rigan bemorlar uchun asosiy davolash usuli bo'lib, bardoshli va samarali davolash usullarini ta'minlaydi [22]. Biroq, immunitetdan qochish hali ham sodir bo'lishi mumkin; Klinik tadqiqotlar ma'lumotlariga ko'ra, melanoma bilan og'rigan bemorlarning 50 va 64 foizi, hatto ipilimumab va nivolumabning kuchli kombinatsiyasi ostida ham, davolanish boshlanganidan keyin 1 va 5 yil ichida kasallikning rivojlanishini boshdan kechiradi [23]. Immunoterapiyaga qarshilikning asosiy mexanizmlarini quyidagicha umumlashtirish mumkin:
PD-L1 (dasturlashtirilgan o'lim-ligand 1) kabi maqsadli molekulalarning saraton hujayralari tomonidan kamayishi, anti-PD-1 (dasturlashtirilgan hujayra o'limi oqsili 1) antikorlarining samaradorligiga xalaqit beradi. Nivolumab va pembrolizumab kabi anti-PD-1 vositalar immun va malign hujayralar o'rtasidagi immunosupressiv o'zaro ta'sirni inhibe qilish uchun mo'ljallangan, bu T-limfotsitlar tomonidan ifodalangan PD-1 va PD o'rtasidagi bog'lanish orqali amalga oshiriladi. -L1, malign hujayralar tomonidan ifodalangan. Binobarin, past PD-L1 ifodasi asosiy qarshilikni ko'rsatadi [24,25].

sistanche o'ti -Antitumor
2. Malign hujayralarning past neoantigen yuki. Neoantigenlar o'simta tomonidan olib boriladigan genetik o'zgarishlardan kelib chiqqan o'ziga xos neoplastik antijenlerdir; o'simta mutatsion yuki qanchalik baland bo'lsa, saraton hujayralari yuzasida taqdim etilgan o'zgartirilgan antijenlarning xilma-xilligi shunchalik ko'p bo'ladi. Ushbu o'zgartirilgan saraton antijenleri mezbon immunitet tizimi tomonidan begona deb tan olinadi, immun infiltratsiyasini va sitotoksiklikni kuchaytiradi. Cheklangan neoantigenlarni tashuvchi o'smalar immun nazoratidan oshib ketishi va immun nazorat nuqtasi inhibitörlerine kamroq javob berishi mumkin [26,27].
3. Immunosupressiya. Saraton hujayralari, shuningdek, miyeloid hosil bo'lgan hujayralar, o'simta stroma hujayralari va CD4 va tartibga soluvchi T limfotsitlar IL-10 (interleykin{{) kabi supressiv sitokinlarning chiqarilishini rag'batlantirish orqali immunitet hujayralarining inaktivatsiyasiga olib kelishi mumkinligi aniqlandi. 4}}) va immun hujayralari infiltratsiyasini va kuchayishini va yallig'lanish sitokinlarini ishlab chiqarishni inhibe qiluvchi TGF-beta (o'simta o'sish omili beta) kabi boshqa kimyoviy vositachilar [28-30]. Shu nuqtai nazardan, mRNK vaktsinasi qarshilik yo'llarini teskari yo'naltiruvchi immun nazorat nuqtasi inhibitörlerine qimmatli qo'shimcha bo'lishga intiladi (1-rasm). mRNK vaktsinalari bilan kodlangan immunitet tizimini stimulyatsiya qilish uchun muhim bo'lgan antijenler (shu jumladan bemorga yoki o'simta turiga xos neoantigenlar va o'simta bilan bog'liq antijenler) antigenni taqdim etuvchi hujayralarning hujayra yuzasida ifodalanishi mumkin, bu esa xost immun tomonidan o'simta uyalarini tanib olishni osonlashtiradi. tizim, tug'ma o'simta neoantigen ishlab chiqarish yoki PD-L1 ifodasidan qat'i nazar [8,9,16]. Bunga parallel ravishda, IL-12, IFN (interferon-alfa), GM-CSF va TLR4 kabi immun faollashuv bilan bog'liq molekulalarni kodlovchi mRNK vaktsinalari saraton hujayralari keltirib chiqaradigan immunitetni susaytirishga qarshi turishi mumkin. immun hujayra faolligini va yallig'lanish vositachisi ishlab chiqarishni tiklash orqali [8,9,16]. Darhaqiqat, yaqinda chop etilgan tajribada bitta zanjirli IL-12 (IL{33}}p40 va IL12p35 subbirliklarining sintezi), IFN-, GM-CSF va IL{{39} uchun mRNK vaktsinasi kodlangan. }}sushi (IL-15 ning IL-15 retseptorining sushi domeniga qo‘shilishi) yo‘g‘on ichak adenokarsinomasi sichqoncha modelida o‘simtani qo‘zg‘atuvchi anti-PD-1 davolashga qarshilikni engishga muvaffaq bo‘ldi. davolash qilingan sichqonlarning qisqarishi va omon qolishini uzaytiradi [31]. Keyinchalik, mRNK vaktsinalari va immun nazorat nuqtasi inhibitörlerini birgalikda qo'llash kelajakdagi terapevtik strategiyaga aylandi [8,9,16]. Maqsadli immunoterapiya immun tizimi bilan yaxshi o'rnatilgan neoplazma bo'lgan melanoma uchun muvaffaqiyatli qo'llanildi [32]. Biroq, metastatik melanoma bemorlarning katta qismi uchun halokatli kasallik bo'lib qolmoqda, bu esa hal qiluvchi davolanish uchun qo'shimcha tadqiqotlar o'tkazish zarurligini keltirib chiqaradi. Immunogen mRNK emlash bu maqsad sari navbatdagi muhim qadam bo'lishi mumkin. Ushbu sharhda biz melanomani davolashda mRNK vaktsinalariga oid so'nggi preklinik va klinik ma'lumotlarni, shuningdek, kelajakdagi istiqbollar va potentsial ilovalarni tasvirlashga harakat qilamiz.

Shakl 1. Immunitetni nazorat qilish punkti immunoterapiyasini kuchaytirishga qaratilgan mRNK vaktsinasining immun tizimi bilan o'zaro ta'sirining sxematik tasviri. TMB: O'simta mutatsion yuki, ICIs: Immunitetni nazorat qilish punkti inhibitörleri.
2. Klinikadan oldingi dalillar
mRNK vaktsinalari turli tajribalarda klinikadan oldingi sichqon saratoni modellarida baholangan (1-jadval). Lipid kaltsiy fosfat nanopartikullari (LCPs) bilan barqarorlashtirish gp100 va tirozinaz bilan bog'liq protein 2 (TRP-2) ni kodlovchi mRNK vaktsinasining samaradorligini oshirishi ko'rsatildi, bu immunokompetent murin B16F10 melanoma modellariga kiritilgan. Emlash o'simtaning sezilarli darajada qisqarishiga olib keldi, shu bilan birga davolangan sichqonlarning omon qolish muddatini uzaytirdi [33].
Jadval 1. mRNK vaktsinalari melanomani davolashda: Klinikadan oldingi ma'lumotlar.

2018 yilda Vang va boshqalar. [34] tirozinaz bilan bog'liq protein 2 (TRP-2) va PD-L1 ifodasini yo'naltiruvchi RNKni (siRNK) o'chirishni o'z ichiga olgan mRNKni o'z ichiga olgan LCP asosidagi vaktsina orqali dendritik hujayralarni in vitro transfeksiyasi muvaffaqiyatli bo'lganligini xabar qildi. TRP-2 melanotsitlarda melanin sinteziga vositachi bo‘lgan oqsil bo‘lib, haddan tashqari ekspressiya qilinganida melanoma hujayralarining DNKni buzuvchi moddalarga qarshilik ko‘rsatishi haqida xabar berilgan [38]. Sichqoncha melanomasi modellari to'g'ridan-to'g'ri emlanganda, limfa tugunlarida, o'simta massasida va taloqda CD8 plyus T limfotsitlar hosil bo'lishi davolanmagan hayvonlarga nisbatan oshdi. T-limfotsitlarga xos TRP-2 reaktsiyasi kuchaytirildi, PD-L1 (dasturlashtirilgan o'lim ligand 1) ifodasi samarali ravishda ishdan chiqdi. Davolangan hayvonlarda o'simta o'sishi, shuningdek, saraton limfa tugunlarining o'sishi sezilarli darajada kechiktirildi. Qizig'i shundaki, TRP{18}}kodlovchi mRNK va siRNK kombinatsiyasi orqali emlash TRP-2 mRNK vaktsinasi va anti-PD{{22} bilan birgalikda qo'llash bilan solishtirganda o'simta o'sishini sezilarli darajada kechiktirishi aniqlandi. } (dasturlashtirilgan hujayra o'limi oqsili 1) monoklonal antikor. Shuningdek, LCP hosil bo'lishi hujayra ichidagi kaltsiyning ajralishi orqali dendritik hujayralarning kamolotini rag'batlantirgani ta'kidlandi. LCP asosidagi boshqa mRNK vaktsinasi, shuningdek, TRP{25}} ni kodlaydi, fagotsitoz orqali antigen taqdim qiluvchi hujayralarni (APC) infiltratsiya qilishga muvaffaq bo'ldi, kuchli T hujayralari faollashuvini qo'zg'atdi va 4-retseptor (TLR4) vositachiligida signal va yallig'lanishni kuchaytirdi. melanoma sichqoncha modellarida teri ostiga yuborilganda sitokin chiqarilishi. Natijada, emlov bilan davolangan sichqonlarda o'simta o'sishi davolanmagan nazoratga qaraganda ancha kechikdi [35]. Sintetik fosforotioat bilan o'zgartirilgan CpG oligodeoksinukleotidlarini (CpG-ODNs) o'z ichiga olgan kombinatsiyalangan vaktsinani o'simta ichiga yuborish singenik murin modellarida o'ziga xos melanoma neoantigenlari uchun immun javobini va mRNK kodlashni kuchaytiradi, shu bilan birga CD8 o'simtasi va CD4 o'simtasida immunofilm o'sishini inhibe qiladi. plyus limfotsitlar [36]. Yaqinda nashr etilgan eksperimentda TRP-2 va tuxum oqi oqsilini kodlovchi mRNK sitotoksik limfotsitlar [39] tomonidan neoantigenni tanib olishni kuchaytirishi ko'rsatilgan, singenik melanoma sichqon modellarining limfa tugunlariga etkazilgan ovalbumin hujayraning sitotoksik reaktsiyasini kuchaytirishga muvaffaq bo'ldi. CD8 plus T hujayralari tomonidan. Bunga parallel ravishda, anti-PD-1 inhibitori bilan birgalikda davolangan sichqonlarning 40 foizida to'liq javoblar kuzatildi. Vaktsinatsiya qayta tiklash urinishlarida uzoq muddatli immun xotiraga olib kelishi ko'rsatilgan, bunda emlangan hayvonlarda metastatik o'sma o'sishi inhibe qilingan [37].

cistanche tubulosa - immunitet tizimini yaxshilaydi
3. Klinik dalillar
mRNK vaktsinalari bir necha faza I/II klinik sinovlari doirasida rivojlangan melanomali bemorlarga qo'llanilgan (2-jadval). 2006-yildayoq otologik monotsitlardan olingan dendritik hujayralardan tashkil topgan vaktsina ex vivo autolog o'simta mRNKsi bilan yuklangan, 22 malign melanomali bemorlarga intranodal yoki intradermal tarzda kiritilgan. T-limfotsitlar kengayishi va interferon ishlab chiqarish bilan tavsiflangan vaktsinaga xos immun reaktsiyasi haqiqatan ham 19 bemordan to'qqiztasida kuzatildi, T hujayralari proliferatsiyasi/interferon-ELISPOT tahlillari bilan baholandi, shuningdek, kechiktirilgan yuqori sezuvchanlik reaktsiyasi bilan baholanadigan 8/18 da. [40]. Intradermal yoki intranodal qo'llash davolangan bemorlarning mos ravishda 70 foizida (7/10) va 25 foizida (3/12) immunitet reaktsiyasini keltirib chiqardi [40]. Keyinchalik [41], javob beruvchilarning to'qqiz nafarida vaktsina mRNK tomonidan kodlangan neoantigenlarga qarshi immunitetga xos CD4 plyus va CD8 plyus T hujayralari javoblari xabar qilindi; Emlashdan so'ng ajratilgan bemorlarning T hujayralari dendritik hujayralarga maxsus reaksiyaga kirishadigan turli xil T-hujayra klonlarini ishlab chiqarishga muvaffaq bo'ldi, shu bilan birga vaktsinaning neoantigen spektrini aks ettiruvchi T hujayra retseptorlarining keng doirasi qayd etildi. Melanoma antijenlarini (Melan-A, Tyrosinase, gp100, MAGE-A1, MAGE-A3, Survivin) kodlovchi protamin-stabillashtirilgan mRNKni 21 ta metastatik melanoma bilan kasallangan bemorlarga [42] to'g'ridan-to'g'ri intradermal yuborish yaxshi muhosaba qilindi va bu darajadagi noxush hodisalarni keltirib chiqarmadi. 3 yoki undan yuqori. Emlangan bemorlarda tartibga soluvchi va miyeloid bostiruvchi hujayralar aylanishi sezilarli darajada cheklangan. Vaktsina antijenlariga qarshi o'ziga xos T-limfotsitlar immun reaktsiyasi baholanadigan to'rtta bemordan ikkitasida qayd etilgan va o'lchanadigan kasallik bo'lgan etti bemordan birida to'liq javob kuzatilgan.
Jadval 2. Melanomani davolashda mRNK vaktsinalari: Klinik ma'lumotlar.
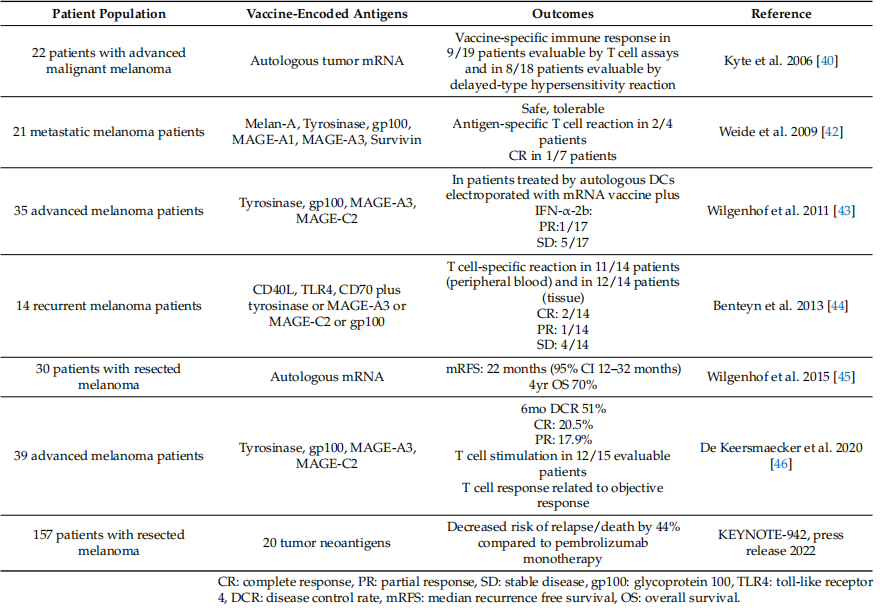
TriMix mRNK vaktsinasi CD40 ligand uchun mRNK kodlashdan iborat (T yordamchi hujayra yuzasi oqsili, antigenga xos reaktsiya vositachisi), konstitutsiyaviy faol toll-o'xshash retseptor 4 (gematopoetik va gematopoetik bo'lmagan hujayra yuzasi antijeni ekzogen va endogenlarni tanib olish vositachisi) va CD70 (o'simta immun nazorat nuqtasi antijeni) turli sinovlarda sinovdan o'tgan. Tajribali tadqiqotda [43] otolog TriMix elektroporatsiyalangan dendritik hujayralar HLA II sinf signali bilan konjugatsiyalangan melanoma bilan bog'liq antigen (MAGE-A3, MAGE-C2, tirozinaza yoki gp100) uchun mRNK kodlash orqali transfektsiya qilindi. Transfektsion dendritik hujayralar 35 bosqich III/IV inoperabl melanoma bemorlariga xavfsiz tarzda qo'llanildi, ammo RECIST mezonlariga muvofiq ob'ektiv javoblar kuzatilmadi. Qo'shimcha IFN{14}}b kiritilgandan so'ng, baholangan bemorlarning 1/17 qismi qisman javobni boshdan kechirdi, 5/17 esa barqaror kasallikni ko'rsatdi. To'rtinchi TriMix-DCs in'ektsiyasidan so'ng 21 bemorda o'tkazilgan teri biopsiyalari ularning 12 tasida emlangan neoantigenga xos T-limfotsitlar tomonidan infiltratsiyani ko'rsatdi. Shunisi e'tiborga loyiqki, melanoma bilan bog'liq antijenler (MAGE-A3, MAGE-C2, tirozinaza, gp100) bilan eritilgan TriMix-DCs bilan otologik emlash periferik qon namunalarida mavjud bo'lgan vaktsinal neoantigenga yo'naltirilgan T limfotsitlarining kengayishiga olib kelishi ko'rsatilgan. /14 va baholangan davolangan bemorlarning 12/14 da teri biopsiyalarida [44]. 14 baholangan bemorlar orasida ikkita to'liq va bitta qisman ob'ektiv javob qayd etilgan, boshqa 4/14 bemorlarda kasallikning barqarorlashuvi qayd etilgan. PFS va OS mos ravishda 1,8 oydan 51 oygacha va 6,4 oydan 51 oygacha o'zgardi; ammo tadqiqotda klinik natija va immunologik javob o'rtasida hech qanday mustahkam bog'liqlik kuzatilmadi [44]. ASCO 2019 [47] da TriMix vaktsinasi yuqori dozali rejimni olgan ilgʻor bosqichli melanomali bemorlarning 4/10ida va past dozali rejimni qabul qilgan bemorlarning 3/9 qismida baholanadigan immun javoblarni keltirib chiqarishi xabar qilingan [47].

Supermen o'tlar cistanche-Antitumor
Xuddi shu TriMix-DC-MEL vaktsinasi, to'rtta melanoma bilan bog'liq antijenler (tirozinaz, gp100, MAGE-A3 va MAGE-C2) uchun mRNK kodlashiga asoslangan, shuningdek, 30 ta ilg'or vaksinada ipilimumab qo'llash bilan birlashtirilgan. melanoma bilan og'rigan bemorlar [46]. Besh yillik umumiy va progressiv omon qolish darajasi mos ravishda 28 va 18 foizni tashkil etdi. Periferik qon mononuklear hujayrasini (PBMC) olish va melanomaga qarshi emlash antijenini boyitish uchun immun javobni baholash 15/30 bemor uchun (mos ravishda CR, PR va SD bilan 4/15, 4/15 va 2/15) mumkin edi. Vaktsinaga immun javob 12/15 bemorlarda qayd etilgan va klinik ob'ektiv javoblar bilan sezilarli darajada bog'liq bo'lib, barqaror yoki progressiv kasallikka chalingan bemorlarga nisbatan qisman va to'liq javoblarga ega bo'lgan bemorlarda kuchliroqdir. Shunisi e'tiborga loyiqki, umumiy omon qolish immun javob beruvchilarda CD8 va T hujayralarining faollashuvi ulushi bilan bog'liq ekanligi aniqlandi [46]. Melanomaga xos antijenler (MAGE-A1, -A3, -C2, tirozinaza, MelanA/MART-1 yoki gp100) uchun mRNK kodli yuklangan otologik dendritik hujayralar va HLA II sinf nishonga olish ketma-ketligi bilan emlash. Shuningdek, 30 rezektsiya qilingan III/IV bosqich melanomali bemorlarda ham baholangan [45]. Xabar qilingan o'rtacha relapssiz omon qolish deyarli ikki yilni tashkil etdi (22 oy; CI 95% 12-32 oy). Nashr qilingan vaqtga kelib, o'n ikki bemor vafot etdi va to'rt yillik umumiy omon qolish darajasi 70 foizni tashkil etdi. O'rtacha umumiy omon qolishga erishilmadi. mRNK vaktsinalariga qo'llaniladigan melanoma bilan bog'liq neoantigen spektrini kengaytirishga urinishda Ping va boshqalar. [48] 471 melanoma to'qima namunasini 812 ta oddiy teri namunasi bilan solishtirgan. Jami beshta potentsial maqsadli o'sma antijeni aniqlandi (PTPRC, SIGLEC10, CARD11, LILRB1, ADAMDEC1); yuqori antigen ifodasi uzoq muddatli OS va DFS, shuningdek, antigen taqdim qiluvchi hujayralar tomonidan yuqori o'simta infiltratsiyasi bilan bog'liq edi. Ushbu besh antijenning saraton hujayralari tomonidan mustahkam ifodalanishi o'simta immunitetining yanada mustahkam infiltratsiyasi va bemorning umumiy omon qolishini yaxshilash bilan bog'liq bo'lsa, ekspressiya darajasining pastligi va omon qolish muddatining qisqarishi immunogen jihatdan "sovuq" melanomalar bilan bog'liq edi. Bunday kuzatuv tadqiqotlari yangi mRNK vaktsinasini yaratish uchun asos bo'lishi mumkin bo'lgan yuqori immunogenik antijenlarni tan olishga yordam berishi mumkin. Hozirgi vaqtda mRNKga qarshi emlash oltita melanoma klinik sinovlarida baholanmoqda, ular allaqachon istiqbolli natijalarni ko'rsatmoqda [49,50]. ASOSIY QAYD-942 (NCT03897881) [33,34], davom etayotgan ochiq yorliqli IIb fazasi sinovi yordamchi davolash sozlamalari bo'yicha ayniqsa quvonarli natijalarni ko'rsatdi. Ushbu tadqiqotda 20 xil mutatsiyaga uchragan neoantigenlarni kodlaydigan moslashtirilgan mRNK vaktsinasi va anti-PD-1 inhibitori pembrolizumabning kombinatsiyasi to'liq rezektsiya qilingan III/IV bosqich melanomasi bo'lgan bemorlarga pembrolizumabni bir vositali davolash bilan solishtirganda qo'llangan. Ishlab chiqaruvchi kompaniya [51] tomonidan e'lon qilingan so'nggi press-relizga ko'ra, mRNK-4157/V940 vaktsinasi bilan birlashtirilgan pembrolizumab bilan adjuvant davo olgan bemorlarda kasallikning qaytalanish yoki o'lim xavfi pastroq bo'lgan bemorlarga nisbatan 44 foizga kamroq ko'rinadi. yagona agentli pembrolizumab bilan davolash (HR=0.56, 95 foiz CI, 0.31-1.08; bir tomonlama p-qiymati=0.0266). Davolash bilan bog'liq jiddiy nojo'ya ta'sirlar pembrolizumabning kombinatsiyalangan va bitta agentli qo'llarida mos ravishda 14,4 va 10 foiz darajasida qayd etilgan [51]. Avstraliyaning Melanoma instituti professori Jorjina Longning KEYNOTE{87}} dastlabki natijalari bo‘yicha tadqiqotchilarning ishtiyoqi haqida fikr yuritar ekan, bu sinov melanoma terapiyasiga nisbatan “penitsillin momentini” yaratishi mumkinligini ta’kidladi [52]. Bundan tashqari, keyingi bosqich sifatida boshlash uchun III bosqich sinovi ham rejalashtirilgan [53]. To'rtta melanoma antijenini: NY-ESO-1, tirozinaz, MAGE-A3 va TPTEni kodlaydigan BNT111 mRNK vaktsinasining xavfsizligi va bardoshliligi I bosqich sinovida baholanmoqda (NCT02410733). Xuddi shu vaktsina boshqa PD-1 ingibitori, semiplimab bilan birgalikda uch qoʻl bilan qiyosiy II faza sinovida (NCT04526899) qoʻllanilmoqda [50]. Tadqiqotchilar monoterapiyani BNT111 vaktsinasi yoki semiplimab bilan ikkala agentning kombinatsiyasi bilan solishtirishga harakat qiladilar, chunki immun nazorat nuqtasi inhibitori refrakter, rezektsiya qilinmaydigan melanomaga qarshi ikkinchi darajali davolash [50]. Memorial Sloan Kettering saraton markazining I bosqichi sinovi ayni paytda IIB-IV bosqich melanomasi boʻlgan bemorlarga TRP uchun kodlangan mRNK vaktsinasi bilan elektroporatsiyalangan Langerhans tipidagi otologik dendritik hujayralar tegishli jarrohlik davolashdan soʻng qoʻllanilishini baholamoqda. (NCT01456104) [50]. Dendritik hujayralarga yuklangan gp100, tirozinaz, PRAME, MAGE-A3, IDO va boshqa o'simta qo'zg'atuvchi mutatsiyalarga asoslangan otologik mRNK vaktsinasi uveal melanoma bilan og'rigan bemorlarga an'anaviy davolash bilan birgalikda, sinovning I bosqichida qo'llanilishi kerak. NCT04335890) [33]. Bundan tashqari, 2023 yilda bemorlarni ishga qabul qilishni boshlash rejalashtirilgan I fazali ochiq yorliqli sinov (NCT05264974) [50], adjuvantga qaramay, kasallikning qaytalanishidan keyin IIIB bosqichdagi mRNK nanopartikulyar o'smaga qarshi emlashning tolerantligini o'rganishga qaratilgan. immunoterapiya. Tadqiqot 2027 yilda yakunlanishi kutilmoqda [50].
4. Xulosa va kelajak istiqbollari

Cistanche qo'shimchasining foydalari - immunitetni qanday mustahkamlash mumkin
Cistanche Enhance Immunity mahsulotlarini ko'rish uchun shu yerni bosing
【Batafsil ma'lumot so'rang】 Email:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
COVID-19 pandemiyasi davrida mRNK vaktsinalari sinchkovlik bilan oʻrganilib, bu zamonaviy texnologiyaning melanomani davolashda innovatsion imkoniyatlarini ochib berdi. Hayvonlar modelidagi tajribalar va klinik sinovlar istiqbolli natijalarni ko'rsatdi va kelgusi yillarda tizimli tadqiqotlar uchun mustahkam zamin yaratdi. KEYNOTE{4}} sinovi, ayniqsa, mRNK vaktsinasini immun nazorat nuqtasi inhibitori bilan birlashtirib, melanoma davolashda navbatdagi muhim yutuqga erishishga intiladi. mRNKga asoslangan saraton terapiyasini o'rganuvchi kelajakdagi laboratoriya va klinik tadqiqotlar uchun muhim yakuniy nuqtalar ideal tarzda quyidagilarni o'z ichiga oladi:
1. Oddiy hujayralarga ta'sir qilmasdan, immun tizimini yanada samarali va o'ziga xos stimulyatsiya qilishga imkon beradigan yuqori immunogen oqsillarni, ya'ni kimokinlarni yoki o'simta bilan bog'liq antijenlarni aniqlash.
2. Erta degradatsiyadan qochib qutuladigan, xavfsiz boshqarilishi, o'z vaqtida ishlab chiqarilishi va keng miqyosda tarqatilishi mumkin bo'lgan barqarorroq mRNK vaktsinalarini ishlab chiqarish uchun bilim va infratuzilma bo'yicha tajribani rivojlantirish.
3. mRNK emlashning immun nazorat punkti ingibitorlari va hatto kimyoterapiya yoki radioterapiya bilan mumkin bo'lgan kombinatsiyalariga tolerantlik; shuningdek, ob'ektiv javob, kasallikning qaytalanishi yoki rivojlanishining oldini olish, umumiy omon qolish va bemorlarning hayot sifati nuqtai nazaridan ularning samaradorligi.
4. Metastatik, adjuvant va neoadjuvant davolash sharoitida, shuningdek, birinchi yoki ikkinchi darajali davolashda va undan tashqarida mRNKga asoslangan emlashlarning klinik foydasi.
Yuqoridagi so'rovlarga javob berish kerakligi sababli, amaliyotchi shifokorlar bemorlarni xabardor qilish, ularga ro'yxatga olinish va hozirgi texnologiyaga asoslangan dori-darmonlarni olish imkoniyatini taklif qilish uchun ishga yollanishdan xabardor bo'lishlari kerak.
Ma'lumotnomalar
1. Brenner, S.; Yakob, F.; Meselson, M. Protein sintezi uchun genlardan ribosomalarga ma'lumot olib boradigan beqaror qidiruv mahsulot. Tabiat 1961, 190, 576–581. [CrossRef] [PubMed]
2. Volf, J.A.; Malone, RV; Uilyams, P.; Chong, V.; Acsadi, G.; Jani, A.; Felgner, PL In vivo sichqoncha mushaklariga to'g'ridan-to'g'ri gen o'tkazish. Fan 1990, 247 Pt 1, 1465–1468. [CrossRef]
3. Baklaushev, VP; Kilpeläinen, A.; Petkov, S.; Abakumov, MA; Grinenko, NF; Yusubalieva, GM; Latanova, AA; Gubskiy, IL; Zabozlaev, F.G.; Starodubova, E.S.; va boshqalar. Lusiferaza ifodasi bioluminesans tasvirini olish imkonini beradi, lekin ko'krak bezi saratonining ortotopik sichqoncha (4T1) modeliga cheklovlar qo'yadi. Sci. Rep. 2017, 7, 7715. [CrossRef] [PubMed]
4. Jenkins, DE; Hornig, YS; Oey, Y.; Dusich, J.; Purchio, T. Immunitet tanqisligi bo'lgan sichqonlarda sut o'smalari va ko'p metastazlarni tez va sezgir in vivo aniqlash imkonini beruvchi bioluminesans inson ko'krak saratoni hujayralari. Ko'krak bezi saratoni Res. 2005, 7, R444–R454. [CrossRef] [PubMed]
5. Konri, RM; LoBuglio, AF; Rayt, M.; Sumerel, L.; Pike, MJ; Yoxanning, F.; Benjamin, R.; Lu, D.; Curiel, DT. Xabarchi RNK polinukleotid vaktsina vektorining xarakteristikasi. Saraton Res. 1995, 55, 1397–1400 yillar.
6. Chjou, WZ; Hoon, DS; Huang, SK; Fuji, S.; Xashimoto, K.; Morishita, R.; Kaneda, Y. RNK melanoma vaktsinasi: inson glikoproteini 100 mRNK immunizatsiyasi orqali o'smaga qarshi immunitetni keltirib chiqarish. Hum. Gen Ther. 1999, 10, 2719–2724. [CrossRef]
7. Bochkovski, D.; Nair, SK; Snayder, D.; Gilboa, E. RNK bilan impulslangan dendritik hujayralar in vitro va in vivo kuchli antigen taqdim qiluvchi hujayralardir. J. Exp. Med. 1996, 184, 465–472. [CrossRef]
8. Shahin, U.; Kariko, K.; Tureci, Ö. mRNKga asoslangan terapevtiklar - yangi dorilar sinfini ishlab chiqish. Nat. Rev. Drug Discov. 2014, 13, 759–780. [CrossRef]
9. Pardi, N.; Xogan, MJ; Porter, FW; Weissman, D. mRNK vaktsinalari - Vaksinologiyada yangi davr. Nat. Rev. Drug Discov. 2018, 17, 261–279. [CrossRef]
10. Polack, FP; Tomas, SJ; Kitchin, N.; Absalon, J.; Gurtman, A.; Lokhart, S.; Peres, JL; Peres Mark, G.; Moreira, ED; Zerbini, C.; va boshqalar. BNT162b2 mRNA COVID-19 vaktsinasining xavfsizligi va samaradorligi. N. Engl. J. Med. 2020, 383, 2603–2615. [CrossRef]
11. Shroff, RT; Chalasani, P.; Vey, R.; Pennington, D.; Quirk, G.; Schoenle, MV; Peyton, KL; Uhrlaub, JL; Ripperger, TJ; Jergovich, M.; va boshqalar. Qattiq o'smalari bo'lgan kattalardagi BNT162b2 mRNK vaktsinasining ikki va uch dozasiga immun javoblari. Nat. Med. 2021, 27, 2002–2011. [CrossRef]
12. Jekson, LA; Anderson, EJ; Rouphael, NG; Roberts, kompyuter; Makene, M.; Koler, RN; McCullough, deputat; Chappell, JD; Denison, MR; Stivens, LJ; va boshqalar. SARS-CoV2d ga qarshi mRNK vaktsinasi haqida dastlabki hisobot. N. Engl. J. Med. 2020, 383, 1920–1931 yillar. [CrossRef]
13. Iavarone, C.; O'xagan, DT; Yu, D.; Delahaye, NF; Ulmer, JB mRNKga asoslangan vaktsinalarning ta'sir qilish mexanizmi. Ekspert Rev. Vaktsinalar 2017, 16, 871–881. [CrossRef]
14. Tomba'ch, I.; Vaysman, D.; Pardi, N. messenjer RNK bilan emlash: DNK vaksinatsiyasiga istiqbolli alternativ. Usullari Mol. Biol. 2021, 2197, 13–31.
15. Miao, L.; Chjan, Y.; Huang, L. saraton immunoterapiyasi uchun mRNK vaktsinasi. Mol. Saraton 2021, 20, 41. [CrossRef]
16. Barbier, AJ; Jiang, AY; Chjan, P.; Vuster, R.; Anderson, DG mRNK vaktsinalari va immunoterapiyaning klinik rivojlanishi. Nat. Biotexnologiya. 2022, 40, 840–854. [CrossRef] [PubMed]
17. Van Nuffel, AM; Wilgenhof, S.; Thielemans, K.; Bonehill, A. Klinik sinovlarda HLA cheklanishini bartaraf etish: mRNK yuklangan DC terapiyasining immun monitoringi. Onkoimmunologiya 2012, 1, 1392–1394. [CrossRef]
18. Xu, S.; Yang, K.; Li, R.; Chjan, L. mRNA vaktsinasi davri mexanizmlari, dori platformasi va klinik prospekt. Int. J. Mol. Sci. 2020, 21, 6582. [CrossRef] [PubMed]
19. Xie, N.; Shen, G.; Gao, V.; Xuan, Z.; Huang, C.; Fu, L. Neoantigens: saraton terapiyasi uchun istiqbolli maqsadlar. Signal uzatish. Nishon. 2023, 8, 9. [CrossRef]
20. Liu, CC; Yang, X.; Chjan, R.; Chjao, JJ; Hao, DJ Tumour bilan bog'liq antijenler va ularning saratonga qarshi qo'llanilishi. Yevro. J. Saraton kasalligini davolash 2017, 26, e12446. [CrossRef] [PubMed]
21. Kosentino, M.; Marino, F. COVID-19 mRNK vaktsinalarining farmakologiyasini tushunish: boshoq bilan zar oʻynashmi? Int. J. Mol. Sci. 2022, 23, 10881. [CrossRef] [PubMed] 22. Bagchi, S.; Yuan, R.; Engleman, EG Saratonni davolash uchun immun nazorat nuqtasi ingibitorlari: Klinik ta'sir va javob va qarshilik mexanizmlari. Ann. Rev. Patol. 2021, 16, 223–249. [CrossRef] [PubMed]
23. Larkin, J.; Chiarion-Sileni, V.; Gonsales, R.; Grob, JJ; Rutkovski, P.; Lao, CD; Koui, CL; Schadendorf, D.; Vagstaff, J.; Dummer, R.; va boshqalar. Kengaytirilgan melanomada Nivolumab va Ipilimumab kombinatsiyasi bilan besh yillik omon qolish. N. Engl. J. Med. 2019, 381, 1535–1546. [CrossRef] [PubMed]
24. Patel, SP; Kurzrock, R. PD-L1 ifodasi saraton immunoterapiyasida bashorat qiluvchi biomarker sifatida. Mol. Saraton Ther. 2015, 14, 847–856. [CrossRef]
25. Fundytus, A.; Booth, CM; Tannock, IF Qanchalik pastga tushishingiz mumkin? PD-L1 ifodasi saraton immunoterapiyasi sinovlarida biomarker sifatida. Ann. Onkol. 2021, 32, 833–836. [CrossRef] 26. Jardim, DL; Gudman, A.; de Melo Gagliato, D.; Kurzrock, R. Immunoterapiya biomarker sifatida o'simta mutatsion yukining qiyinchiliklari. Saraton hujayrasi 2021, 39, 154–173. [CrossRef]
27. Chan, TA; Yarchoan, M.; Jaffee, E.; Swanton, C.; Quezada, SA; Stenzinger, A.; Peters, S. Immunoterapiya biomarker sifatida o'sma mutatsion yukining rivojlanishi: Onkologiya klinikasi uchun yordam. Ann. Onkol. 2019, 30, 44–56. [CrossRef]
28. Long, H.; Jia, Q.; Vang, L.; Fang, V.; Vang, Z.; Jiang, T.; Chjou, F.; Jin, Z.; Xuan, J.; Chjou, L.; va boshqalar. O'simtadan kelib chiqqan eritroid prekursorlari bilan differentsiatsiyalangan miyeloid hujayralar immunosupressiyaga vositachilik qiladi va anti-PD-1/PD-L1 davolash samaradorligini pasaytiradi. Saraton hujayrasi 2022, 40, 674–693.e7. [CrossRef]
29. Garsiya Garsiya, CJ; Huang, Y.; Fuentes, NR; Turner, MC; Monberg, ME; Lin, D.; Nguyen, Shimoliy Amerika; Fujimoto, TN; Chjao, J.; Li, JJ; va boshqalar. Stromal HIF2 oshqozon osti bezi saratoni mikro muhitida immunitetni bostirishni tartibga soladi. Gastroenterologiya 2022, 162, 2018–2031. [CrossRef]
30. Vu, Y.; Yi, M.; Niu, M.; Mei, Q.; Wu, K. Miyeloiddan olingan bostiruvchi hujayralar: saratonga qarshi immunoterapiya uchun yangi maqsad. Mol. Saraton 2022, 21, 184. [CrossRef]
31. Bernardo, M.; Tolstix, T.; Chjan, YA; Bangari, DS; Cao, H.; Heyl, KA; Li, JS; Malkova, NV; Malley, K.; Markes, E.; va boshqalar. Anti-PD-1 qarshilikning eksperimental modeli TGFß va Notch yo'llarining faollashuvini namoyish etadi va mahalliy mRNK immunoterapiyasiga sezgir. Onkoimmunologiya 2021, 10, 1881268. [CrossRef] [PubMed]
32. Tucci, M.; Passarelli, A.; Mannavola, F.; Felichi, C.; Stucci, LS; Cives, M.; Silvestris, F. Melanoma rivojlanishining belgisi sifatida immun tizimidan qochish: Dendritik hujayralarning roli. Old. Onkol. 2019, 9, 1148. [CrossRef] [PubMed]
33. Oberli, MA; Reyxmut, AM; Dorkin, JR; Mitchell, MJ; Fenton, OS; Yaklenik, A.; Anderson, DG; Langer, R.; Blankschtein, D. Lipid nanopartikulyar mRNKni kuchli saraton immunoterapiyasi uchun yetkazib berish. Nano Lett. 2017, 17, 1326–1335. [CrossRef] [PubMed]
34. Vang, Y.; Chjan, L.; Syu, Z.; Miao, L.; Huang, L. mRNK vaktsinasi antigenga xos nazorat punkti blokadasi o'rnatilgan melanomaga qarshi kuchaytirilgan immunitet reaktsiyasini keltirib chiqaradi. Mol. U erda. 2018, 26, 420–434. [CrossRef]
35. Chjan, X.; Siz, X.; Vang, X.; Cui, L.; Vang, Z.; Xu, F.; Li, M.; Yang, Z.; Liu, J.; Huang, P.; va boshqalar. Lipidga o'xshash material bilan mRNK vaktsinasini etkazib berish Toll-o'xshash retseptor 4 signalizatsiyasi orqali o'smaga qarshi ta'sirni kuchaytiradi. Proc. Natl. akad. Sci. AQSh 2021, 118, e2005191118. [CrossRef]
36. Li, Q.; Ren, J.; Liu, V.; Jiang, G.; Xu, R. CpG oligodeoksinukleotidi Primatlarning immun javoblarini faollashtirish uchun ishlab chiqilgan neoantigenga asoslangan mRNK saratoniga qarshi vaktsina bilan birgalikda antitumoral ta'sirni kuchaytiradi. Drug Des. Dev. U erda. 2021, 15, 3953–3963. [CrossRef]
37. Chen, J.; Ye, Z.; Huang, C.; Qiu, M.; Song, D.; Li, Y.; Xu, Q. Lipid nanopartikullar vositachiligida limfa tuguniga mo'ljallangan mRNK saratoniga qarshi vaktsina yetkazib berish mustahkam CD8 va T hujayralari javobini keltirib chiqaradi. Proc. Natl. akad. Sci. AQSh 2022, 119, e2207841119. [CrossRef] [PubMed]
38. Chu, V.; Pak, BJ; Bani, MR; Kapur, M.; Lu, SJ; Tamir, A.; Kerbel, RS; Ben-David, Y. Tyrosinase bilan bog'liq protein 2 sis-diamminedichloroplatinum (II) ga melanomaga xos qarshilik vositachisi sifatida: Terapevtik ta'sir. Onkogen 2000, 19, 395–402. [CrossRef]
39. U, M.; Huang, L.; Xou, X.; Zhong, C.; Bachir, ZA; Lan, M.; Chen, R.; Gao, F. Maqsadli melanoma immunoterapiyasi uchun yangi ko'p funktsiyali mitselyar platforma yordamida samarali ovalbumin etkazib berish. Int. J. Pharm. 2019, 560, 1–10. [CrossRef]
40. Kyte, JA; Mu, L.; Aamdal, S.; Kvalxaym, G.; Dueland, S.; Xauzer, M.; Gullestad, HP; Rayder, T.; Lislerud, K.; Hammerstad, H.; va boshqalar. Otolog o'simta-mRNK bilan transfektsiyalangan dendritik hujayralar bilan melanoma terapiyasining I/II bosqichi sinovi. Saraton geni. 2006, 13, 905–918. [CrossRef]
41. Kyte, JA; Kvalxaym, G.; Lislerud, K.; Tor Straten, P.; Dueland, S.; Aamdal, S.; Gaudernack, o'simta-mRNK transfektsion dendritik hujayralar bilan emlashdan so'ng melanomali bemorlarda G. T hujayralari javoblari. Saraton immunol. Immuno-boshqa. 2007, 56, 659–675. [CrossRef]
42. Weide, B.; Paskolo, S.; Scheel, B.; Derxovanessian, E.; Pflflugfelder, A.; Eigentler, TK; Pavelec, G.; Xoer, I.; Rammensee, HG; Garbe, C. Protamin bilan himoyalangan mRNKni to'g'ridan-to'g'ri in'ektsiya qilish: metastatik melanomali bemorlarda 1/2 fazali emlash sinovi natijalari. J. Immunother. 2009, 32, 498–507. [CrossRef] [PubMed]
43. Vilgenhof, S.; Van Nuffel, AM; Kortals, J.; Heirman, C.; Tuyaerts, S.; Benteyn, D.; De Konink, A.; Van Riet, I.; Verfailli, G.; Vandeloo, J.; va boshqalar. Rivojlangan melanoma bilan og'rigan bemorlarda otolog mRNK elektroporatsiyalangan dendritik hujayrali vaktsina bilan terapevtik emlash. J. Immunother. 2011, 34, 448–456. [CrossRef] [PubMed]
44. Benteyn, D.; Van Nuffel, AM; Wilgenhof, S.; Kortals, J.; Herman, C.; Neyns, B.; Thielemans, K.; Bonehill, A. mRNK elektroporatsiyalangan otolog dendritik hujayralar (TriMixDC-MEL) bilan davolangan melanomali bemorlarning periferik qonida va teri in'ektsiya joylarida CD8 plus T-hujayra javoblarining tavsifi. Biomed Res Int. 2013, 2013, 976383. [CrossRef]
45. Vilgenhof, S.; Kortals, J.; Van Nuffel, AM; Benteyn, D.; Heirman, C.; Bonehill, A.; Thielemans, K.; Neyns, B. Metastazlarning to'liq rezektsiyasidan so'ng xabarchi RNK-elektroporatsiyalangan dendritik hujayra terapiyasi bilan davolangan melanomali bemorlarning uzoq muddatli klinik natijalari. Saraton immunol. Immuno-boshqa. 2015, 64, 381–388. [CrossRef] [PubMed]
46. De Keersmaecker, B.; Klerxout, S.; Karrasko, J.; Bar, I.; Kortals, J.; Wilgenhof, S.; Neyns, B.; Thielemans, K. TriMix va o'simta antijeni mRNK elektroporatsiyalangan dendritik hujayrali emlash va ipilimumab: T-hujayra faollashuvi va rivojlangan melanomada klinik javoblar o'rtasidagi bog'liqlik. J. Immunother. Saraton 2020, 8, e000329. [CrossRef]
47. Arance Fernandes, AM; Baurain, J.-F.; Vulsteke, C.; Rutten, A.; Soria, A.; Karrasko, J.; Neyns, B.; De Keersmaecker, B.; Van Asshe, T.; Lindmark, B. Rezektsiya qilingan melanomali bemorlarda TriMix asosidagi mRNK immunoterapiyasining (ECI-006) I bosqichi (E{2}}MEL): Xavfsizlik va immunogenlik tahlili. J. Klin. Onkol. 2019, 37, 2641. [CrossRef]
48. Ping, H.; Yu, V.; Gong, X.; Tong, X.; Lin, C.; Chen, Z.; Cai, C.; Guo, K.; Ke, H. mRNK vaktsinasini ishlab chiqish uchun melanoma o'simtasi antijeni va immun subtiplarini tahlil qilish. Tekshirish. Yangi dorilar 2022, 40, 1173–1184. [CrossRef]
49. Lorentzen, CL; Haanen, JB; Met, Ö.; Svane, IM Klinik yutuqlar va saraton kasalligini davolash uchun mRNK vaktsinalari bo'yicha davom etayotgan sinovlar. Lancet Onkol. 2022, 23, e450–e458. [CrossRef]
50. ClinicalTrials.gov. Onlaynda mavjud: https://www.clinicaltrials.gov/ (2023-yil 10-yanvarda kirilgan).
51. Moderna va Merck mRNK-4157/V940, tadqiqot uchun moslashtirilgan mRNK saratoniga qarshi vaktsinani KEYTRUDA® (Pembrolizumab) bilan birgalikda, 2b-bosqichda KEYNOTE-942 sinovida birlamchi samaradorlikning yakuniy nuqtasiga mos kelishini e'lon qildi. Onlaynda mavjud: https://www.merck.com/news/moderna-and-merck-announce-mrna-4157-v940-an-investigational-personalized-mrna saraton-vaccine-in-combination- with-keytruda-pembrolizumab-met-primary-efficacy-endpoint-in-phase-2b-keynote-94/ (2022-yil 13-dekabrda kirish).
52. Melanoma uchun mRNK vaktsinalarida yutuq. Onlaynda mavjud: https://www1.racgp.org.au/newsgp/clinical/breakthrough in-mrna-vaccines-for-melanoma (kirish 2023-yil 10-yanvar).
53. mRNK vaktsinasi Plus KEYTRUDA® Melanoma omon qolishini yaxshilaydi. Onlaynda mavjud: https://www.europeanpharmaceuticalreview. com/news/177505/mrna-vaccine-plus-keytruda-improve-melanoma-survival/ (2023-yil 10-yanvarda kirilgan).
