Koronavirus kasalligi 19 (COVID-19) ga qarshi nuklein kislotaga asoslangan vaktsina platformalari
Aug 11, 2023
Abstrakt
Koronavirus kasalligi 2019 (COVID-19) pandemiyasi 673 010 496 bemorni yuqtirgan va bugungi kunga qadar butun dunyo bo'ylab 6 854 959 kishining o'limiga sabab bo'lgan. Bir-biridan tubdan farq qiladigan COVID{8}} vaktsina platformalarini ishlab chiqish uchun katta sa'y-harakatlar qilindi. mRNK va DNK vaksinalaridan tashkil topgan nuklein kislotasi asosidagi vaksinalar (uchinchi avlod vaktsinalari) tez va qulay ishlab chiqarish hamda COVIDga qarshi immunitetni samarali qoʻzgʻatish nuqtai nazaridan istiqbolli boʻlib kelmoqda-19. Bir nechta DNKga asoslangan (ZyCoV-D, INO-4800, AG{15}}COVID19 va GX-19N) va mRNKga asoslangan (BNT162b2, mRNA-1273 va ARCoV) tasdiqlangan vaktsina platformalaridan COVID-19 oldini olish uchun foydalanilgan. mRNK vaktsinalari COVID-19 oldini olish boʻyicha barcha platformalarda birinchi oʻrinda turadi. Biroq, bu vaktsinalar past barqarorlikka ega, DNK vaktsinalari esa immunitetni rag'batlantirish uchun yuqori dozalarda talab qilinadi. Nuklein kislotaga asoslangan vaktsinalarni hujayra ichiga yuborish va ularning nojo'ya hodisalari qo'shimcha tadqiqotlarni talab qiladi. Xavotirga sabab boʻlgan COVID-19 variantlari qayta paydo boʻlganini hisobga olsak, vaktsinalarni qayta baholash va polivalent vaktsinalar yoki pan-koronavirus strategiyalarini ishlab chiqish infektsiyani samarali oldini olish uchun zarur.

Cistanche qo'shimchasining foydalari - immunitetni qanday mustahkamlash mumkin
Cistanche Enhance Immunity mahsulotlarini ko'rish uchun shu yerni bosing
【Batafsil ma'lumot so'rang】 Email:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Kalit so'zlar
Koronavirus kasalligi 19 · Nuklein kislota asosli vaktsinalar · Immunitet · Himoya
Fon
2019 yil oxirida Xitoyning Uxan shahrida yangi beta-koronavirus paydo bo'ldi va butun dunyoga tez tarqaldi. Koronavirus kasalligi 2019 (COVID-19) dunyo miqyosida yuqori oʻlim darajasiga ega boʻlgan yuqumli kasallik darajasi tufayli pandemiyaning yuqori potentsialiga ega (Sharma va boshq. 2020; Su va boshq. 2020; Wibawa 2021). Shuning uchun kasallikka qarshi samarali vaktsinalar yoki davolash usullarini ishlab chiqish uchun katta harakatlar talab etiladi (Su va boshq. 2020). COVID-19 kasalligining alomatlari turlicha boʻladi, jumladan, engil fuga oʻxshash simptomlar, pnevmoniya, oʻtkir respirator distress sindromi (ARDS) va oʻlimga olib keladigan natija. Saraton, qandli diabet, yurak-qon tomir kasalliklari, keksa odamlar va hatto genetik moyilligi bo'lgan bemorlarda COVID-19 og'irligining eng yuqori xavfi mavjud (Sharma va boshq. 2020; Su va boshq. 2020; Wibawa 2021; Vakil va boshq. 2022). Jahon sogʻliqni saqlash tashkiloti (JSST) tavsiyalariga koʻra, niqob kiyish, virusga qarshi dorilarni qoʻllash, ijtimoiy masofani saqlash va emlash tartib-qoidalariga rioya qilish butun dunyo boʻylab COVID{14}} pandemiyasini nazorat qilishda muhim xatti-harakatlardir (Sharma va boshq. 2020). Invaziv patogenlarga qarshi samarali vaktsinalarni ishlab chiqish bo'yicha ilmiy urinishlar uzoq yillar davomida boshlangan (Deb va boshq. 2020; Zhang va boshq. 2020; Wibawa 2021). Ushbu vaktsina platformalari patogen bakteriyalarga qarshi ham ishlab chiqilgan (Farhani va boshq. 2019; Jafari va Mahmoodi 2021). Shu nuqtai nazardan, samarali, himoya va xavfsiz vaktsinani ishlab chiqish og'ir o'tkir respirator sindromli koronavirus 2 (SARS-CoV-2) tarqalishiga to'sqinlik qiluvchi asosiy profilaktika usuli hisoblanadi (Mur va Klasse 2020). Shu sababli, dunyo boʻylab turli farmatsevtika kompaniyalari va tadqiqot guruhlari xalqaro hamjamiyatda foydalanish uchun COVID{25}}ga qarshi xavfsiz va samarali vaksinani taqdim etish uchun raqobatlashdi. Ushbu sa'y-harakatlar klinikadan oldingi va klinik sinovlarga kirish uchun boshqa vaktsina platformalarini ishlab chiqdi va ularning ba'zilari ma'qullandi (Chen va boshq. 2021), jumladan, jonli yoki inaktivatsiyalangan, subunit va nuklein kislotasi asosidagi vaktsinalar kabi an'anaviy vaktsinalar keyingi avlod vaktsinalari sifatida. (Mur va Klasse 2020). Ilmiy dalillarga asoslanib, jonli zaiflashtirilgan vaktsinalar uzoq muddatli immunitetga ega bo'lgan Tollga o'xshash retseptorlarni (TLR) qo'zg'atish orqali tug'ma, hujayrali va gumoral immunitet reaktsiyalarini rag'batlantiradi va yuqori sezuvchanlikni rivojlanishi mumkin. Ushbu vaktsinalarning asosiy kamchiliklari ularning xavfsizligi va samaradorligini baholashdir. Inaktivatsiyalangan virusli vaktsinalar hujayra immunitetini zaif tarzda qo'zg'atadi, bu ularning samaradorligini pasaytiradi. 2020-yil aprel oyida Sinovac va Vuxan biologik mahsulotlar instituti (Sinopharm) tomonidan inaktivatsiyalangan COVID{34}} vaksinasi ishlab chiqarilgan (Moore and Klasse 2020; Su va boshq. 2020). Subunit vaktsinalar xavfsizdir, ba'zi kamchiliklari past immunogenlik, kuchaytiruvchi yoki yordamchi talab va yuqori narxga ega (Koirala va boshq. 2020; Su va boshq. 2020). Nuklein kislotasi asosidagi vaktsinalar ketma-ketlik ma'lumotlari asosida ishlab chiqilgan. Ular turli dozalarda hujayra va gumoral immun javoblarni kuchli rag'batlantiradigan antijenlarning DNK yoki mRNK ketma-ketligini o'z ichiga oladi. Tez ishlab chiqarish va klinik sinovlardagi eng birinchi COVID{40}} vaktsinalari kabi afzalliklari tufayli DNKga asoslangan vaktsinalarning sezilarli afzalligi ularning turli saqlash sharoitlarida barqarorligidir (Silveira va boshq. 2020; van Riel va de. Aqlli 2020). RNK asosidagi vaktsinalar Pfizer/Biotech va Moderna kabi farmatsevtika kompaniyalarining e'tiborini tortdi. DNK vaktsinalaridan farqli o'laroq, ular adjuvantsiz TLR ligandlari sifatida samarali gumoral immun javobni rag'batlantiradilar va ularning ketma-ketligi mRNK degradatsiyasini oldini olish uchun o'zgartiriladi (Moore and Klasse 2020; van Riel va de Wit 2020; Soiza va boshq. 2021). Ushbu sharh nuklein kislotasi asosidagi vaksinalar, jumladan, COVIDga qarshi mRNK va DNK vaksinalaridagi soʻnggi ishlanmalarni baholashga qaratilgan edi-19.
Asosiy matn
Koronavirus infektsiyasining molekulyar mexanizmi va immun javobi

cistanche o'simlik - immunitet tizimini oshiradi
COVID-19 genomi konvert (E), boshoq (S), membrana (M) va nukleokapsid (N) dan iborat to'rtta asosiy strukturaviy oqsillarni kodlaydigan ijobiy bir zanjirli RNKdir (Stadler va Rappuoli 2005), 1a-rasmda ko'rsatilgandek. Inson SARS-CoV konvertning bir qismi sifatida spike (S) glikoproteinini o'z ichiga oladi. Virusning xost hujayralariga qo'shilishi S1 va S2 bo'linmalaridan iborat boshoq oqsili tomonidan amalga oshiriladi. Ular infektsiyani boshlash uchun angiotensin-konverting ferment II (ACE2) deb nomlanuvchi hujayra retseptorlari bilan bog'lanishda muhim rol o'ynaydi (1b-rasm). S1 domenining ACE2 ga yuqori yaqinlik bilan bog'langan markaziy hududi retseptorlarni bog'lovchi domen (RBD) hisoblanadi. Shu munosabat bilan, RBD va ACE2 o'rtasidagi o'zaro ta'sir inson hujayra infektsiyasini boshlash uchun talab qilinadi (He va boshq. 2020). Bundan tashqari, S proteinining kesilishi virusning xost hujayralariga kirishi uchun zarurdir; RBD hududi ACE2 ga biriktirilgandan so'ng, TM proteaz serin 2 (TMPRSS2) deb nomlanuvchi xost proteazasi S proteinini S1 va S2 domenlariga ajratadi, bu esa S2 domeni xost hujayrasiga birlashishiga olib keladi (Huang va boshq. 2020). Kuchli immun javoblar COVID-19, yuqori sezuvchanlik va sitokin bo'roniga (asosan interleykin-6-, IL-1b, GM-CSF-, interferon- / IFN -, nekroz omiliga) qarshi samarali bo'lsa-da. TNF -, IL-10-, IL-2- va IL- 7-javoblari) taqiqlanishi kerak (Chowdhury va boshq. 2020). Virusning biriktirilishi (boshoq-ACE2 o'zaro ta'siri) va nafas olish hujayralariga kirishdan so'ng, fagotsitar alveolyar makrofaglar va dendritik hujayralar (DC) virus antijenlarini T hujayralariga taqdim etadi va T CD4+(yordamchi T hujayra) va T CDni faollashtiradi{{37} }} (sitotoksik T hujayra). Keyinchalik, virus bilan uchrashish uchun IL6, IL12, TNF va IFN va boshqalar kabi yallig'lanishga qarshi sitokinlar chiqariladi. Biroq, sitokin bo'roniga olib keladigan sitokin ishlab chiqarishning yuqori darajasi o'pkaning shikastlanishiga olib keladi (Hosseini va boshq. 2020). Ilmiy dalillarga ko'ra, yordamchi T hujayralari virusli infektsiyani yo'q qilish, antikorlarni ishlab chiqarish uchun B hujayralarini induktsiya qilish va sitotoksik T hujayralarini rag'batlantirish uchun zarurdir (Sharma va boshq. 2020). COVID-19 antijenik maqsadlari Patogen organizmga qarshi xavfsiz va himoya qiluvchi vaktsinani ishlab chiqishda eng yaxshi immunogen maqsadlarni aniqlash muhim (Lu va boshq. 2020b). Potentsial antijenik maqsadlarni qabul qilish hujayra va gumoral immunitetni to'g'ri qo'zg'atish uchun T hujayralari va B hujayra epitoplarini qo'zg'atish uchun juda muhimdir (Rueckert va Guzman 2012). Virusli S oqsili asosiy ligand sifatida RBD domeni orqali xost hujayralari bilan o'zaro ta'sir qiladi. RBD domeni neytrallashtiruvchi antikor ishlab chiqarishni va COVIDga qarshi T-hujayra immun javobini keltirib chiqarishi mumkin-19. Shuningdek, S proteinining immunogenligi tasdiqlangan (Pushparajah va boshq. 2021). N oqsili boshqa virusli oqsillarga nisbatan kichik va yuqori darajada saqlanib qolgan ketma-ketlikka ega. N proteini virus infektsiyasi vaqtida yuqori darajada ifodalanadi va bemorlarda COVID-19ga qarshi sezilarli gumoral immun javob beradi. Bundan tashqari, N proteiniga qarshi hujayrali javoblar bilan uni vaktsinani loyihalashda mos nomzod antijen deb hisoblash mumkin (Dutta va boshq. 2020). Bundan tashqari, M oqsili va E proteini T CD{50}}epitoplarini rag'batlantiradi (Vang va boshq. 2005; Abdelmageed va boshq. 2020; Dong va boshq. 2020). S oqsiliga qarshi kuchli immun javoblarni keltirib chiqarish hal qiluvchi va zarurdir (Buchholz va boshq. 2004). S oqsili eng immunogen T-hujayra va B hujayra epitoplarini oʻz ichiga oladi, chunki u COVID-ga qarshi vaktsina yaratishda afzal koʻriladigan maqsad sifatida tanilgan-19. U Pfizer/BioNtech va Moderna vaktsinalari kabi barcha ishlab chiqilgan mRNK platformasi vaktsinalarida qo'llanilgan.

1-rasm a SARS-CoV-2 virion tuzilishi; COVID-19 virusining asosiy sirt oqsillariga Spike (S) glikoprotein, Membran (M) va Zarf (E) oqsillari kiradi. S proteini asosiy vaktsina va terapevtik maqsad bo'lib, infektsiyani boshlash uchun angiotensin-konverting ferment II (ACE2) retseptorlari bilan o'zaro ta'sir qiladi. b boshoq oqsilining domenlari; S oqsiliga S1 (NTD yoki tarjima qilinmagan domen va RBD yoki retseptorlarni bog'lovchi domen) va S2 subbirliklari kiradi.
Nuklein kislotaga asoslangan dorilar tarixi
Oligonukleotidlar 30 yildan ko'proq vaqt oldin klinik sinovlarga kiritilgan. Nuklein kislotasiga asoslangan terapevtik yondashuvlardan foydalanish tarixi 1977 yilda Paterson va boshq. gen ifodasini moslashtirish uchun nuklein kislotalardan foydalangan (Paterson va boshq. 1977). Hozirda ular ko'proq e'tiborga olindi. Nuklein kislotaga asoslangan dorilar turli toifalarga bo'linadi, jumladan, antisens shakllari, ribozimlar, mRNK va DNKga asoslangan vaktsinalar (Sharma va boshq. 2014). Sintetik oligodeoksinukleotid RSV mRNK ni to'ldiruvchi va antisens sifatida tanilgan Rous Sarkoma Virusining (RSV) replikatsiyasini inhibe qilgan (Zamecnik va Stivenson 1978). Birinchi antisens sitomegalovirusga (CMV) qarshi klinikaga kiritilgan (Mulamba va boshq. 1998). Kichik interferent RNK (siRNK) gen ekspressiyasini inhibe qilish potentsialiga ega va birinchi marta 1998 yilda xabar qilingan. Kichik kodlamaydigan RNKlarning yana bir guruhiga gen ekspressiyasini tartibga solishda ajralmas rolga ega bo'lgan mikroRNKlar (miRNKlar) kiradi. siRNK va terapevtik salohiyatga o'xshash funktsiyalar (Usman va Blatt 2000; Sharma va boshq. 2014). Yuqorida aytib o'tilganidek, RNK molekulalarining ribozim sinfi transkripsiyani maqsad qilgan fermentlar vazifasini bajaradi. Ribozimlar saraton va inson immunitet tanqisligi virusi (OIV) kabi ba'zi virusli infektsiyalarga qarshi klinik sinovlarga kirishdi (Usman va Blatt 2000; Abera va boshq. 2012). mRNK va DNKga asoslangan vaktsinalarga qo'shimcha ravishda ular 1990-yilda kiritilgan nuklein kislotasi asosidagi dori vositalarida tasniflanadi va COVID bilan kurashish uchun vaktsinalarni ishlab chiqishga ko'proq e'tibor qaratildi-19 (Le va boshq. 2020; Zhang va boshq. 2020). Ushbu vaktsina guruhlarining asosiy afzalliklari ularning tez ishlab chiqarilishi va mos keladigan maqsadli antijenlarga nisbatan yuqori o'ziga xosligini o'z ichiga oladi (Le va boshq. 2020).

cistanche tubulosa - immunitet tizimini yaxshilaydi
mRNKga asoslangan vaktsinalar
mRNK molekulalarini xost hujayralariga dastlabki etkazib berish katyonik lipid yordamida fibroblast hujayralariga mRNK transfeksiyasini o'z ichiga oladi (Park va boshq. 2021). mRNK vaktsinalari inson hujayralari tomonidan antijenik oqsillarni ishlab chiqaradigan patogen antijenler mRNKni o'z ichiga oladi. mRNK vaktsinalarining bir qancha afzalliklari orasida oddiy ishlab chiqarish jarayoni, samarali va himoyalangan immunitet, qulay manipulyatsiya va sanoatlashtirish hamda COVID-19 variantlariga javob berish moslashuvchanligi kiradi (Kaufman va boshq. 2016; Fang va boshq. 2022). Ba'zi yondashuvlar, masalan, 5'-kap va Kozak ketma-ketliklarini qo'shish, 3'-poli-A ketma-ketliklari va mRNK nukleozidlarini o'zgartirish yordamida qo'llaniladi (Borah va boshq. 2021). mRNK vaktsinalari mezbon sitozolga aylantiriladi. Shuning uchun genomlarni joylashtirish xavfi yo'q, bu ularning asosiy afzalligi sifatida tanilgan. Shu munosabat bilan, mRNKga asoslangan vaktsinalar yaqinda saraton va yuqumli kasalliklarga qarshi xavfsiz profilaktika yondashuvi sifatida ko'proq e'tiborga sazovor bo'ldi (Kaur va Gupta 2020). mRNK vaktsinalarining asosiy ta'sir mexanizmi 2-rasmda tasvirlangan.
DNKga asoslangan vaktsinalar
DNK vaktsinalari plazmid vektorlari tomonidan ifodalangan va elektroporatsiya (EP) orqali hujayralarga uzatiladigan virusli antijenik peptidlarni kodlaydigan bir nechta genlarni o'z ichiga oladi. Boshqa vaksina platformalari bilan taqqoslaganda, DNK vaksinalari vaksinalarni ishlab chiqish uchun moslashuvchan va tezkor platformani taklif qiladi, bu esa uni COVID-19 kabi rivojlanayotgan epidemiyalarga qarshi kurashishning ajoyib texnologiyasiga aylantiradi. Bundan tashqari, DNK vaktsina antijeni ishlab chiqarish maqsadli hujayralarda sodir bo'ladi, bu virusli antigenning tabiiy konformatsiyasini va translatsiyadan keyingi modifikatsiyasini qayta tiklashga yordam beradi. DNK vaktsinalarining asosiy kamchiligi ularning cheklangan immunogenligidir. Shu sababli, DNK vaktsinasining salohiyatini oshirishi mumkin bo'lgan yordamchi yoki asosiy kuchaytiruvchi rejimdan foydalanish kabi strategiyalarni ko'rib chiqish muhimdir. Bundan tashqari, nuklein kislotani xost DNKsiga integratsiya qilish onkogenez va mutagenezga olib keladigan yana bir bioxavfsizlik muammosidir (Rauch va boshq. 2018). Oldingi tadqiqotlarga ko'ra, DNK vaktsinasini kiritish xavfi ahamiyatsiz bo'lsa-da, JSST va FDA integratsiya uchun DNK vaktsina xavfsizligini amalga oshirishni tavsiya qiladi (Vang va boshq. 2004; Schalk va boshq. 2006). DNK vaktsinalari koronavirus genlarini inson hujayralariga o'tkazadi. Emlash printsipi DNKning hujayra yadrosiga etkazib berilishiga bog'liq bo'lib, antigen transkripsiyasi boshlanadi va keyin tarjima qilinadi. DNK vaktsinalari odatda plazmidlarni vektor sifatida ishlatadi. Vaktsinani yuborish yo'lidan kelib chiqqan holda, miyositlar va keratinotsitlar ko'rib chiqiladi. Shu bilan birga, in'ektsiya joyi yaqinidagi antigen taqdim qiluvchi hujayralar ham DNK vaktsinalari yordamida to'g'ridan-to'g'ri transfektsiya qilinishi mumkin. Bunday hollarda, o'zaro faoliyat astarlash jarayoni ikkala asosiy gisto-moslashuv kompleksi (MHC-I/II) molekulalaridan foydalangan holda antijenlarni ifodalaydi (Hobernik and Bros 2018). Yaratilgan antijenler apoptotik tanalar yoki ekzosomalar yordamida chiqariladi, bu esa ularni antigen taqdim qiluvchi hujayralar tomonidan tan olinishiga olib keladi, bu esa o'z navbatida hujayra va gumoral immunitet reaktsiyalarini qo'zg'atadi. Kuchli immunitet reaktsiyasini yaratish uchun turli xil etkazib berish strategiyalari qo'llaniladi (Donnelly va boshq. 2005; Li va Petrovskiy 2016; Strizova va boshq. 2021). COVID{14}} infektsiyasi paytida immunitetni tartibga solishga kelsak, noto'g'ri prognozli perikardial efüzyon xavfi ostida bo'lgan bemorlarda CD3+CD8+ ko'tarilgan CD8+ T hujayralari va kamaygan CD{{ 18}}HLA-DR va T tartibga soluvchi (Treg) hujayralari (Duerr va boshq. 2020). Bu natijalar shuni ko'rsatadiki, og'ir infektsiya kasallik sharoitlarini yanada kuchaytiradigan nomutanosib immunitet reaktsiyasi tufayli yuzaga keladi (Tay va boshq. 2020). COVID{22}} vaktsinasining rivojlanishi bunday nomutanosiblikka erishmasdan samarali va mos immun javobini (jumladan, ikkala qoʻlni ham) rivojlantirishga qaratilgan (Hobernik and Bros 2018). Odamlarda DNK vaktsinalarining klinik sinovlari umumiy javoblarni keltirib chiqargan bo'lsa-da, bu javoblar qabul qilinadigan klinik afzalliklarni tezlashtirish uchun ko'pincha etarli emas. Bundan tashqari, plazmid DNKning asosiy komponentlari, masalan, metillanmagan CpG ketma-ketliklari tug'ma immun javoblarning faollashishiga olib kelishi mumkin, bu esa ifodalangan antijenlere qarshi adaptiv immun javoblarni oshiradi. Shunday qilib, DNK vaktsinalari veterinariya tibbiyotida ko'proq qo'llaniladi (Coban et al. 2013; Silveira et al. 2017; Hobernik and Bros 2018). Ushbu kamchilik tufayli, ba'zi tadqiqot yo'nalishlari DNK vaktsinalarini optimallashtirish va etkazib berishga qaratilgan, jumladan, kodon optimallashtirish, promotor dizayni, molekulyar adjuvantlar, EP qo'llash, prime-boost emlash yoki ilg'or vaktsina dizayni uchun "omiks" usullari (Li va boshqalar. 2012; Silveyra va boshqalar 2020). 3-rasmda DNK vaktsina mexanizmlarining asosiy bosqichlari samarali immun reaksiyalarida tasvirlangan.

2-rasm mRNK vaktsinasi formulasi, qo'llanilishi va immun provokatsiyasi mexanizmlari: lipid nanozarracha (LNP) bo'lgan mRNK formulasi ketma-ketlik barqarorligini saqlaydi va kuchaytiradi. b mRNK-LNP vaktsinasining fiziologik eritmasi mushak ichiga yuboriladi. c LNP o'z ichiga olgan mRNK endositoz orqali antigen taqdim qiluvchi hujayralarga (APC) o'tkaziladi. mRNK sitoplazmada chiqariladi va virus oqsillariga aylanadi, so'ngra ular proteazoma tomonidan parchalanadi va endoplazmatik retikulum yuzasida asosiy gistologik moslashuv kompleksi I (MHC-I) bilan bog'lanadi va T sitotoksik (Tc) hujayralariga taqdim etiladi.
mRNK va DNKga asoslangan vaktsinalarning salohiyati
mRNK darajasidagi vaktsina tuzilishi barqarorlik va oqsil ifodasini tiklash uchun elementlarni o'z ichiga oladi, shu jumladan 3'UTR, kodlash ketma-ketligi, 5'UTR, 5' qopqoq va poli (A) dum (Liu 2019). Virusli yoki eukaryotik genlardan olingan kodlash ketma-ketligini qo'llab-quvvatlaydigan 5' va 3' UTR elementlari vaktsinalar uchun muhim omillar bo'lgan mRNKning strukturaviy barqarorligini oshiradi va tarjimasini yaxshilaydi (Ross va Sullivan 1985; Holtkamp va boshq. 2006). mRNK dan oqsillarni samarali tarjima qilish uchun 5 ′ qalpoqli struktura kerak (Martin va boshq. 1975; Ross va Sullivan 1985). mRNK poli (A) dumi ham mRNK barqarorligi va tarjimasida tartibga soluvchi rolga ega (Holtkamp va boshq. 2006). Bundan tashqari, kodondan foydalanish oqsillarni tarjima qilishda muhim rol o'ynaydi. Shu munosabat bilan, mRNK dan oqsil translatsiyasini oshirish uchun noyob kodonlar sitozolda ko'p turdagi tRNKga ega bo'lgan sinonimik kodonlar bilan almashtiriladi (Stepinski va boshq. 2001). Tartibni optimallashtirishning yana bir yondashuvi G: C tarkibini boyitishdir. So'nggi yillarda samarali va xavfsiz nomzod DNK vaktsinalarini bir necha usullar ishlab chiqdi. DNKga asoslangan vaktsinalar platformasida bakterial kelib chiqadigan plazmid vektorlari xost hujayralari ichida kerakli antijenlarni ifodalash uchun qo'llaniladi. Bakterial plazmidlar eukaryotik hujayralarga kirib, yadroga ko'chirilishi kerak. Keyin DNK transkripsiyalanadi va mos ravishda mezbon hujayraning yadrosi va sitoplazmasidagi begona genlardan tarjima qilinadi. Shuning uchun, yuqori transfeksiya samaradorligi va oqsil ifodasi bilan to'g'ri plazmidni loyihalash kuchli DNK vaktsinasiga erishish uchun juda muhimdir (Malone va boshq. 1989). Eukaryotik mintaqaning ketma-ketligi (DNK vaktsinalari plazmidlarida), kiritilgan genning yuqori oqimi, antigenik ketma-ketlikning 3' uchida joylashgan promotor va poli A signalidan (polyA) (AAU AAA) iborat (Shan va boshqalar. 2011). Promotorlar DNK vaktsina plazmidlarida zarur bo'lgan muhim elementlar bo'lib, xost hujayralarida kerakli antijenlarning yuqori ifoda darajasini qo'zg'atadi (Becker va boshq. 2008) va kiritilgan gendan mRNK transkripsiyasiga olib keladi. DNK vaktsinalarida eng ko'p ishlatiladigan promouter inson sitomegalovirusi (CMV) promouterini o'z ichiga oladi. PolyA ketma-ketlik signali mRNK barqarorligi va uzatish va eukaryotik genlarning samarali ifodalanishiga olib keladi. Yana bir muhim element bu eukaryotik ribosoma tomonidan tarjima qilishda muhim rol o'ynaydigan Kozak ketma-ketligi (ACCATGG). Shuningdek, bir yoki ikkita stop-kodon ketma-ketligini qo'shish xost hujayrasida kiritilgan genning noto'g'ri tarjimasini oldini olish uchun zarurdir (Becker va boshq. 2008; Uilyams 2013). DNK va mRNK vaktsina platformalarini taqqoslash Garchi DNK va mRNK vaktsinalari 1990-yillardan beri ishlab chiqilayotgan bo'lsa va yaqinda ishlab chiqilgan va turli veterinariya DNK vaktsinalari litsenziyalangan bo'lsa-da, katta ishtiyoq mRNKga aylandi. Ikkalasi ham plazmid DNK va mRNKni to'g'ridan-to'g'ri manipulyatsiya qilish yoki immunomodulyatorlar yoki adjuvantlar, formulalar va etkazib berish tizimlarini qo'shish orqali ularning antigenligi, barqarorligi va samaradorligini oshirish uchun harakatlarni talab qiladi (Liu 2019). mRNKning barqarorlik davomiyligi plazmid DNKnikiga qaraganda pastroq. DNK vaktsinalari yuqori ichki plazmid DNK barqarorligi tufayli mRNK vaktsinalariga qaraganda ko'proq miqdorda kodlangan oqsilni tezda hosil qilishi aniqlandi. Plazmid DNK mushakda 6 oygacha integratsiyalanmagan rejimda saqlanib qolishi aniqlandi (Ledwith va boshq. 2000). DNK va mRNK vaktsinalari sevimli oqsilni ifodalash tizimi bo'lishi kerak bo'lsa-da, ularning hech biri immunologik inert emas. Shuningdek, DNK plazmidlari va mRNK tug'ma immunitetni rag'batlantiradi (Kampbell 2017). DNK va mRNKga asoslangan vaktsina texnologiyasi umuman umumiy bo'lmasligi mumkin. mRNK o'zgartirilgan nukleozidlar va etkazib berish uchun zarur bo'lgan formulalar, barqarorlik va mRNKning ichki immunostimulyator faolligini nazorat qilish zarurati tufayli plazmid DNKga qaraganda murakkabroq. Shunga qaramay, u har bir uyali yoki hayvonot mahsulotiga bo'lgan talabdan qochadigan ishlab chiqarishga foyda keltiradi. Va'da shundan iboratki, plazmid DNK va mRNK vaktsinasi bilan bog'liq muammolar, ayniqsa kasalliklarning oldini olish va davolash uchun ilg'or texnologiyalarni qo'llash orqali hal qilingandan so'ng klinik yutuqlar amalga oshirilishi mumkin (Liu 2019).

3-rasm. Antigen taqdim qiluvchi hujayralarga (dendritik hujayralar yoki DC) COVID-19 DNK vaktsinasini ifodalash jarayoni. Plazmid DNK DC yadrosiga kiradi va in vivo antigenlarni ifodalaydi (1) Keyin antigenlar MHC-I va MHC-II molekulalari orqali T hujayralariga (T hujayra retseptorlari yoki TCR) taqdim etiladi. Antigen taqdimoti DC CD80/{7}} molekulalari va MHC-I-TCR bilan birga CD8+T hujayra CD28 molekulalari, shuningdek DC CD40 va CD{13}}T hujayra CD40L bilan birga sodir bo'ladi. MHC-II-TCR o'zaro ta'siri (2a, 3 va 4) CD8+T hujayralari va sitokinlar chiqarilishining faollashishi va ko'payishi makrofaglarning faollashishi (2b) kabi samarali immun javoblariga olib keladi. Bundan tashqari, CD faollashishi. 4+DK larning sitokinlar bilan bogʻlanishi va taʼsiridan soʻng T hujayralari B hujayralarining faollashishi, koʻpayishi va antikorlar sekretsiyasi bilan bogʻliq (5)
DNK va mRNK vaktsinasini yetkazib berishdagi taraqqiyot
Eukaryotik hujayralar tomonidan begona DNK va RNK o'zlashtirilishi virusli vektorlarga nisbatan samarali emas. Hujayralarni qabul qilish qobiliyatini oshirish uchun ko'plab jismoniy etkazib berish yondashuvlari yaratilgan (Mellott va boshq. 2013). Genlarni transfeksiya qilishning fizik usullari genetik materialni mexanik protseduralar, shu jumladan EP va proyektor qurilmalari orqali uzatuvchi etkazib berish tizimlarini o'z ichiga oladi (Gulce-Iz va Saglam-Metiner 2019). Biojektor qurilmalari CO2 bosimidan terapevtik moddalarni IM (mushak ichiga), ID (deri ichiga) va shuningdek, SC (teri ostiga) yuborish orqali igna talabisiz (Jorritsma va boshq. 2016) o'tkazish uchun foydalanadi, bu an'anaviy igna in'ektsiyasiga nisbatan sezilarli afzalliklarni beradi, shu jumladan in'ektsiyani yumshatadi. salbiy ta'sirlar, igna o'zaro kontaminatsiyasi va igna tayoqchasining shikastlanishi (Zhang va boshq. 2015). Tegishli ravishda, ikkita DNK vaktsinasi Zika virusiga qarshi I bosqichda sinovdan o'tkazildi, bu igna ishlatish bilan solishtirganda ignasiz yuborishdan keyin hujayrali javoblarning kuchayganligini ko'rsatdi (Gaudinski va boshq. 2018). Bundan tashqari, proyektor yordamida quturganlarga qarshi mRNK vaktsinasini etkazib berish platformasi antikorlarning yaxshilangan javoblarini aniqladi (Alberer va boshq. 2017). Reaktiv in'ektsiya orqali vaktsina samaradorligining oshishi vaktsinalarning kengroq taqsimlanishi bilan bog'liq bo'lishi mumkin, bu esa APClar yordamida yuqori qabul qilinishiga olib keladi (Williams va boshq. 2000; Alberer va boshq. 2017). Hozirgi vaqtda ID yoki IM in'ektsiyalaridan keyin EPdan keyin odatda klinik tadqiqotlarda DNK vaktsinasini yuborish uchun foydalaniladi (Sardesai and Weiner 2011). EP elektr impulslari yordamida genetik materialning hujayra o'zlashtirilishini oshirish uchun teri hujayralari ichida gözenek shakllanishini o'z ichiga oladi (Pushparajah va boshq. 2021). IM EP usuli birinchi navbatda 1998 yilda qo'llanilgan (Aihara 1998), DNK vaktsinalarini etkazib berish uchun mushak hujayralarining penetratsiyasini oshirish (Rizzuto va boshq. 1999; Dupuis va boshq. 2000; Sokołowska va Błachnio-Zabielska 2019). Ko'pgina hisobotlar EP yordamida antigenning yaxshi ifodalanishini va antigenga xos immun javoblarning kuchayganligini aniqladi (Yan va boshq. 2008; Yan va boshq. 2009). OIV DNK vaktsinasi ADVAX IM orqali yuborilgandan so'ng immunogenlikni oshirganligi haqida xabar berilgan (Vasan va boshq. 2011), IM yuborish bilan solishtirganda (Vasan va boshq. 2010). Shunga qaramay, EP yondashuvi yuqori kuchlanishlardan foydalanish tufayli hujayra o'limi xavfidan aziyat chekadi (Gulce-Iz va Saglam-Metiner 2019). EP kabi yangi yetkazib berish yondashuvlari RNK vaktsinasini yetkazib berish uchun hali tekshirilmayapti.

Cistanche erkaklar uchun foydalari-immun tizimini mustahkamlaydi
O'z-o'zini kuchaytiruvchi vaktsinani etkazib berish bo'yicha EP samaradorligi sichqonlarda gen ifodasi va immun javoblari nuqtai nazaridan plazmid DNK vaktsinalariga o'xshash edi (Cu va boshq. 2013). Biroq, RaI an'anaviy takrorlanmaydigan RNK vaktsinalarining etkazib berish samaradorligini oshirmadi (Johansson va boshq. 2012), ehtimol uning RNK vektorlarini ko'paytirishda samaradorligini pasaytiradi. Shunga koʻra, EP va bioinjektorlar COVID-19 DNK/RNK vaktsinalarini parenteral yuborish uchun foydalidir. Ushbu yondashuvlar DNK vaktsina nomzodlarini ishlab chiqarish va etkazib berishni oshirishga yordam beradi va natijalarni sezilarli darajada yaxshilaydi (Pushparajah va boshq. 2021).
Nuklein kislotaga asoslangan vaktsinalarning afzalliklari va cheklovlari
Immunizatsiyaning yangi va istiqbolli usullari sifatida nuklein kislotasi asosidagi vaktsinalar COVID-19 pandemiyasi davrida millionlab odamlar tomonidan namoyish etilganidek, xavfsiz va himoyalovchi emlashni ishlab chiqish haqida tushuncha beradi (Choi and Chang 2013). Nuklein kislotasi asosidagi vaktsinalar qisqa rivojlanish davrlariga ega bo'lib, pandemiya paytida tez tarqalishni osonlashtiradi. Rekombinant DNK vaktsinalaridan foydalanish DNK vektorini yadroga samarali o'tkazish, transkripsiya va keyin kerakli antigenga tarjima qilishni talab qiladi (Leitner va boshq. 1999). Qulay manipulyatsiya va arzon ishlab chiqarish tufayli yalang'och plazmid DNK antijenlarni taqdim etish uchun ajoyib vektordir (Williams 2013). Odatda, plazmid DNK asosiy genetik elementlarni o'z ichiga oladi, jumladan antigenni kodlovchi gen, promotor, kuchaytirgichlar va transkripsiyani tugatish/poliadenilatsiya ketma-ketligi (Vogel va Sarver 1995). Plazmid DNK platformasi - bu tozalashni talab qilsa ham, arzon prokaryotik hujayralar ichida yuqori darajada takrorlanadigan istiqbolli biofarmatsevtik konstruktsiyadir (Prazeres va boshq. 1999; Ferreira va boshq. 2000; Suschak va boshq. 2017). RNK vaktsinalari 3′, poli-A dum va 5′ uchlari bilan o'ralgan antigen RNKni o'z ichiga olgan mRNK molekulalaridan iborat bo'lib, transkripsiyaga ehtiyoj sezmaydi. (Zhang va boshq. 2019). Bir nechta RNK vaktsinalari ishlab chiqilayotgan yangi texnologiya deb nomlanuvchi o'z-o'zini kuchaytiradi. Shunga ko'ra, RNK molekulasi yalang'och RNKning beqarorligi ehtimoliga qaramay, etkazib berilgandan keyin xostda ko'paytirilishi va tarjima qilinishi mumkin, bu esa immunogen peptidlarning ifodasini oshiradi (Pardi va boshq. 2018; Zhang va boshq. 2019; Wadhwa va boshq. 2020). . mRNK hamma joyda tarqalgan ribonukleaza fermentlari tomonidan parchalanadi (Wadhwa va boshq. 2020; Xu va boshq. 2020). 3' poli-A dumi va 5'-7-metilguanozin qopqog'ining qo'shilishi sitozoldagi mRNKning barqarorligi va tarjimasini oshirish uchun juda muhimdir (Gallie 1991; Schlake va boshq. 2012). Vaktsinani qabul qilish va ekspressiyani oshirish strategiyalari RNK vaktsinalariga qaraganda asosan DNK vaktsinalari uchun baholangan, chunki DNK yadroga kirish uchun ikkita hujayra membranasini kesib o'tishni talab qiladi. Aksincha, RNK sitoplazmaga bitta membrana orqali kiradi (Rauch va boshq. 2018). DNK tuzilishi nisbatan yuqori barqarorlikka ega. 7 yil davomida plazmid DNK −20 darajada saqlangan yangi DNK bilan farq qilmasdan butunligicha qolganligi aniqlandi (Walther va boshq. 2013; Pushparajah va boshq. 2021). Past pH va harorat uzoq vaqt davomida DNK yaxlitligini saqlab qolish uchun juda muhimdir. Aksincha, RNK haroratga juda sezgir va uning yarim umrini oshirish uchun fermentsiz muhitda -70 darajada saqlanishi kerak (Jones va boshq. 2007).
Nuklein kislotaga asoslangan vaktsinalarni ishlab chiqishdagi qiyinchiliklar
Ma'lumki, COVID-19 vaktsinalari etarlicha samarali va himoya bo'lishi kerak (Graham 2020) va uzoq umr ko'radigan immunitetni keltirib chiqaradi. Biroq, grippga qarshi yillik emlash tajribalari asosida yillik emlash mumkin bo'lishi mumkin (Randolph and Barreiro 2020; van Riel and de Wit 2020). COVID-19 vaktsinasini ishlab chiqish hatto yangi platformalarda ham qiyinchiliklar tugʻdiradi. Koronavirus spike protein vaktsinasining yuqori immunogenligi va himoyasiga qaramay, mutatsiyalarning paydo bo'lishi tashvish va virusning qayta paydo bo'lishiga olib keladi. Demak, kasallikning paydo bo'lish vaqti va joylashuvi prognozi va maqsadli oqsil ketma-ketligini aniq qabul qilish klinik sinovlarni to'g'ri amalga oshirishni talab qiladigan rivojlanish jarayonining birinchi bosqichidir (Lurie va boshq. 2020). DNK vaktsinalarining asosiy muammosi odamlarda va yirik hayvonlarda kichik hayvonlar tizimlariga qaraganda nisbatan pastroq immunitet reaktsiyalarini keltirib chiqarishdir (Grunwald va Ulbert 2015; Suschak va boshq. 2017). Shunisi e'tiborga loyiqki, COVID{10}}ga qarshi vaksinalar bilan bog'liq qo'shimcha muammolarni hal qilish kerak, masalan, himoyalanish chidamliligi, muayyan kichik guruhlardagi samaradorlik, virus tarqalishining oldini olish va jamoatchilik tomonidan qabul qilinishi (Pushparajah va boshq. 2021). O'z-o'zini kuchaytiruvchi mRNK vaktsinalaridagi kechiktirilgan antigen ekspressiyasi bu vaktsinalarning samaradorligini cheklashi mumkin. Biroq, bu platforma yuqori hosil beradi va shuning uchun sezilarli darajada past dozalarda ekvivalent himoyani ta'minlaydi (Vogel va boshq. 2018; Strizova va boshq. 2021).
COVID-19 DNK va mRNK vaktsinalaridagi so'nggi yutuqlar
COVID{0}} ga qarshi vaktsina ishlab chiqishda koʻplab tadqiqotlar mRNK vaktsina platformalariga (Verbeke va boshq. 2021) qaratilgan boʻlib, bir nechta vaksinalar (Vitiello va Ferrara 2{{) tasdiqlangan. 94}}21) Moderna va Pfizer/ BioNtech kompaniyalari kabi. Moderna vaktsinasi COVID-19 spike glikoprotein mRNK kodlashini, Pfizer/BioNtech esa RBD mRNK ketma-ketligini o'z ichiga oladi (Brüssow 2020). Pfizer/BioNTech va Moderna vaktsinalarining samaradorlik darajalari mos ravishda 95% va 94,5% ni tashkil qiladi (Rauch va boshq. 2021; Widge va boshq. 2021). Moderna vaktsinasini saqlash harorati -25 daraja va -15 daraja, Pfzer vaktsinasiniki esa -80 daraja va -60 daraja (Meo va boshq. 2021; Rauch va boshq. 2021). Moderna vaktsinasi bilan solishtirganda, Pfizer/BioNTech vaktsinasi arzonroq narx va yon ta'sirga ega (Rauch va boshq. 2021). COVID{17}}ga qarshi yana bir mRNK vaktsina xitoylik tadqiqotchilar tomonidan ishlab chiqilgan va termostabil (kamida bir hafta 25 darajada) RBD kodlovchi mRNKdan foydalanilgan (Brüssow 2020). Boshqa soʻrovda CureVac oqsil barqarorligini yaxshilash uchun ikkita prolin qoldigʻidagi oʻrinbosarlari bilan COVID-19 vaktsinasini ishlab chiqish uchun ishlab chiqilgan toʻliq uzunlikdagi S proteinli mRNK platformasi sifatida ishlatilgan (Rauch va boshq. 2021). Ruklanthi de Alwis va boshqalar. (2021) toʻliq uzunlikdagi S proteini va replikon (de Alwis va boshq. 2021) yordamida COVID{26}} uchun oʻz-oʻzidan transkripsiyalanuvchi va replikatsiyalanuvchi mRNK vaktsinasini ishlab chiqdi (de Alwis va boshq. 2021), samarali va xavfsiz bir dozali vaktsina sifatida qoʻllanilishi mumkin. COVID bilan kurashish- 19 (de Alwis va boshq. 2021). Xuddi shunday, lipid nanozarrachalari (LNP) ichiga oʻralgan COVID{33}} S oqsilini kodlovchi oʻz-oʻzini kuchaytiruvchi RNK ishlatildi va antikor va hujayra immunitetining yuqori titrlarini belgilab berdi (McKay va boshq. 2020). SARS-CoV uchun S, N va M oqsiliga asoslangan vaktsinalar kabi ba'zi DNK vaktsina nomzodlari ishlab chiqilgan. Ular orasida S proteiniga asoslangan DNK vaktsinasi, ehtimol, retseptorlarni bog'lashda S oqsilining muhim roli tufayli COVID{38}} infektsiyasiga qarshi samarali himoya ta'sirini keltirib chiqardi (Chjao va boshq. 2020). INO-4800 bu COVID-19 DNK vaksinasiga nomzod boʻlib, COVID-19 S proteinini kodlaydi (Sarwar va boshq. 2020; Smit va boshq. 2020). Sichqonlar va gvineya cho'chqalarida klinikadan oldingi natijalar gumoral va hujayrali immunitet reaktsiyalarini ko'rsatdi. Klinik tadqiqotlarning I bosqichida INO ning ikki dozasi -4800 ID yo'li orqali yuborildi, CELLECTRA®2000 Inovio Pharmaceutical orqali EP bilan qo'shildi (Diehl va boshq. 2013; Amante va boshq. 2015). To'liq immunitet reaktsiyasi I bosqich klinik sinovining 36 ishtirokchisidan 34 tasida antikor va hujayrali javoblar asosida tushuntirildi. O'nta nojo'ya ta'sirlar (AE) hech qanday jiddiy nojo'ya hodisalarsiz (SAE) kuzatilgan (faza). INO ning immunogenligi, xavfsizligi va bardoshliligini baholash uchun I/II bosqich klinik sinovi boshlandi- 4800 (Tebas va boshq. 2019). INO-4800 oʻxshash saqlash sharoitlariga ega (Smit va boshq. 2020), vaktsinani oddiyroq tarqatishga umid qiladi. Bundan tashqari, COVID{56}}ga qarshi DNK vaksinalarining boshqa baʼzi guruhlari sinovdan oʻtkazildi. 2020-yil iyun oyida GX-19 uchun I va IIa klinik sinov bosqichi ishga tushirildi. Osaka universiteti (Yaponiya), Takaro Bio va AnGes hamkorligida ishlab chiqarilgan DNK vaktsinasi AG0301-COVID-19 2020-yil iyul oyida I va II bosqich klinik sinovlari uchun ishga qabul qilishni boshladi. uning immunogenligi va xavfsizligi (Speiser va Bachmann 2020). ZyCoV-D ning uchta dozasining immunogenligi va xavfsizligini baholash uchun I va II bosqich klinik sinovlari o'tkazildi (Kumar va boshq. 2021). Ushbu og'iz vaktsina plazmid DNKdagi boshoqli oqsilni kodlagan, jonli Bifidobacterium longum, yaxshi tan olingan ichak probiyotik bakteriyasida dinamik ravishda kuchaytirilgan. CORVax12, spike oqsilini kodlovchi DNK vaktsinasini baholash uchun I klinik sinovning yana bir bosqichi boshlandi. Elektroporatsiyalangan CORVax12 ning yakka o'zi yoki interleykin 12 ni (IL{69}}) kodlovchi boshqa plazmid bilan birgalikda samaradorligi o'rganildi. Turli xil COVID{70}} mRNK vaksinalari ishlab chiqilmoqda va istiqbolli natijalarni taqdim etdi (Leitner va boshq. 1999; Croyle va boshq. 2001). RQ{73}}VLP (S, E va M oqsillarini kodlash) yaratishga turlicha yondashuv mRNK kokteyli yordamida in vivo samarali bo‘ldi. Ushbu mRNK vaktsinasi o'zgartirilgan nukleozidlar bilan birlashtirilgan va keyin LNPga qadoqlangan va sichqonlarda kuchli hujayrali va gumoral immun javoblarni keltirib chiqarish qobiliyatini ochgan (Le va boshq. 2020; Lu va boshq. 2020a). Elektroporatsiya yordamida 60 mkg dan ikki dozada ishlab chiqilgan arginil-glisil-aspartik kislota (RGD) domenli DNK vaktsinasi BALB/cJ sichqonlarida ta'sirni yaxshiladi (Guo va boshq. 2021). Bir dozada (0,2 mg) DNK vaktsinasining IM + reaktiv in'ektsiyasi Suriya hamsterlarini immunizatsiya qilishi mumkin (Brocato va boshq. 2021). Uch dozada o'tkazilgan S proteinidan foydalangan holda boshqa DNK vaktsinasi Rhesus makakalarini himoya qildi (Yadav va boshq. 2021). RBD ning gepatit B virusi preS1 amino-terminaliga qo'shilishi va C57BL/6 sichqonlarida uchta dozada (0, 2 va 4-haftalar) IM in'ektsiyasi gumoral va hujayrali immunitet reaktsiyalarini keltirib chiqardi (Jeong va boshq. 2021). Bundan tashqari, Rhesus makakalarida 0, 2 va 8-haftalarda S protein plazmid DNK va S1 subunitini (rekombinant oqsil) uch dozada IM in'ektsiyasi neytrallashtiruvchi antikorlarni rag'batlantirdi (Prompetchara va boshq. 2021). ICR sichqonlarida S proteinini uch dozada (0, 2 va 4-haftalar) IM + EP in'ektsiyasi gumoral va hujayrali javoblarni rag'batlantirdi (Li va boshq. 2021). Klinik tadkikotlardagi boshqa DNK vaktsinalari 2022 yil iyun oyida I/II fazalarida S proteinini o'z ichiga olgan (NCT04445389, 18-50 yoshli kattalardagi IM yo'nalishi), 2021 yil iyul (NCT04463472, 20-60 yoshli kattalardagi IM yo'nalishi), 2021 yil sentyabr (NCT04527081, 20–65 yoshli kattalar uchun IM yoʻnalishi) va I bosqich (NCT04336410, 18 yosh va undan kattalar uchun ID yoʻnalishi), 2022 yil fevral (NCT04334980, 18 yosh va undan kattalar uchun ogʻiz orqali) va 202-iyun NCT04591184, 18-84 yoshdagi kattalardagi IM yo'nalishi). Bundan tashqari, klinik tadkikotlardagi mRNK vaktsinalari 2021 yil noyabrda II faza (NCT04515147, IM, 18–60 yosh), 2022 yil dekabrdagi II-III bosqich (NCT04368728, 18–85 yoshli kattalardagi IM) va I fazani oʻz ichiga olgan. 2021 yil iyun oyida (NCT04566276, 18-75 yoshdagi kattalarda IM). COVID-eVax RBD asosidagi vaktsina boʻlib, 38 kundan soʻng sichqonlar, paromlar va kalamushlarda yetarlicha immun reaktsiyasini keltirib chiqardi (Conforti va boshq. 2022). Spike va nukleokapsid oqsillarini kodlovchi ikkita (X{141}} va GX-19N) DNK vaksinalari 19–49 yoshdagi kattalar oʻrtasida I bosqich sinovlarida baholandi va bogʻlovchi antikorlar emlashning ikkinchi dozasida aniqlandi. GX{145}}N yuqori darajadagi T-hujayralar va antikor reaktsiyalarini keltirib chiqargan bu vaktsinalarning xavfsizligi va bardoshliligi tasdiqlandi (Ahn va boshq. 2022). Xcl1-SARS-CoV-2 spike termoyadroviy DNK vaktsinasi in vitro va in vivo sharoitda plazmid o'z ichiga olgan spike geni bilan solishtirganda antikor va T hujayra vositachiligidagi javoblarning yuqori tezligini keltirib chiqardi (Qi va boshq. 2022). Yaqinda yaratilgan bakuloviral COVID-19 Delta DNK vaksinasi sichqonlarni 100% COVIDdan himoya qilishi mumkin-19 (Jang va boshq. 2023). SARS-CoV-2 RBD (Lin-COVIDeVax) ni kodlovchi chiziqli DNK (linDNA) antikor va T hujayra javoblarini keltirib chiqara oldi va xavfsizlikni ta'minladi va salbiy ta'sir ko'rsatmadi (Conforti va boshq. 2023). 1-jadvalda klinik sinovlar va tasdiqlangan nuklein kislotasi asosidagi COVIDga qarshi vaksinalar-19 keltirilgan. Yangilangan maʼlumotlarga koʻra, butun dunyo boʻylab 229 820 324 kishi COVID{167}}ga qarshi vaktsina olgan, ular orasida Afrika mamlakatlaridagilar ham emlash darajasi pastroq (https://www.usnews.com/news/coronavirus-and). -vaccine-news, https://www.bloomberg.com/graph ics/covid-vaccine-tracker-global-distribution/). Shunga ko'ra, emlash darajasi turli mintaqalar / hududlarning iqtisodiy sharoitlari bilan bog'liq.
COVID-19 vaktsinalari uchun potentsial xavfsizlik muammolari
Har bir ishlab chiqilgan profilaktik yoki profilaktik vaktsinada xavfsizlikni nazorat qilish muhim jihatlardan biridir. mRNK vaktsinasi ishlab chiqarish jarayonlarida zaharli kimyoviy moddalar yoki hujayra madaniyatidan foydalanish talab qilinmaydi, shuning uchun xavfsiz platforma sifatida tanilgan. Qisqa ishlab chiqarish vaqti mikroorganizmlar tomonidan ifloslanish xavfini ham kamaytiradi (Vang va boshq. 2020). Eng ko'p xabar qilingan ta'sirlar orasida bosh og'rig'i, charchoq va boshqa tizimli og'ir hodisalar, masalan, isitma, titroq, miyalji, qusish, qorin og'rig'i va kam uchraydigan diareya xabarlari kiradi. Biroq, mRNK vaktsinasini qabul qiluvchilarda o'lim kuzatilmagan (Chapin-Bardales va boshq. 2021; Skowronski va De Serres 2021). Ba'zi tizimli nojo'ya ta'sirlar, masalan, anafilaksi, odatda allergiya tarixi bo'lgan odamlarda qayd etiladi va million dozaga 2,5-11,1 holatda baholanadi (Shimabukuro va boshq. 2021). Boshqalarga qaraganda yoshroq odamlarda kuchli immunitet reaktsiyasi yuqori tizimli hodisalarga olib kelishi mumkin va birinchi dozaga nisbatan ikkinchi vaktsina kiritilgandan keyin ko'proq nojo'ya ta'sirlar haqida xabar beriladi (Erkak 2021; Skowronski va De Serres 2021). Bundan tashqari, in'ektsiya joyidagi og'riq, qizarish va shishish eng ko'p mahalliy yon ta'sir sifatida qayd etilgan (Anand and Stahel 2021). Pfizer/BioNTech va Moderna kabi tasdiqlangan mRNK vaktsinalarining yetarli dalillariga asoslanib, homiladorlikda abort qilish xavfi (=0%) aniqlanmagan (Erkak 2021). Shunisi e'tiborga loyiqki, DNK vaktsinalari etarlicha xavfsiz, ammo har doim ham immunogen emas; shuning uchun etarli immun javob qo'shimcha dozalarni talab qiladi. Humoral immunitet reaktsiyasi inson sinovlarida izchil bo'lmagan, uyali immunitet esa keng tarqalgan. Shunga ko'ra, keksa va yosh populyatsiyalar orasida DNK vaktsinalarining xavfsizligi yanada qulayroqdir (Ledgerwood va boshq. 2011; Houser va boshq. 2018; Carter va boshq. 2019). Xavfsizlik masalalari transfektsion DNKning germline va xostning somatik hujayralariga integratsiyalashuviga ishora qiladi. Bunday hollarda gen ekspressiyasini tartibga solishning buzilishi bir nechta muhim mutatsiyalar bilan birga sodir bo'lishi mumkin. Shunga qaramay, odatda DNK vaktsinasini ishlab chiqishda faqat ekstraxromosomali va etishmayotgan xromosoma integratsiya plazmidlari qo'llaniladi. Bundan tashqari, ko'pchilik plazmidlar administratsiya joyida qoladi (Schalk va boshq. 2006). Yaqinda o'tkazilgan tizimli ko'rib chiqish va meta-tahlil shuni ko'rsatdiki, mRNK vaktsinalari boshqa platformalarga nisbatan yuqori noxush hodisalar bilan bog'liq (Kouhpayeh and Ansari 2022). Yaqinda 34- yoshli ayolda BNT162b2 mRNK vaktsinasi bilan bog'liq miyozitning kamdan-kam holatlari kuzatildi (Magen va boshq. 2022). DNK metilatsiyasi va tegishli epigenetik o'zgarishlar ham DNK va mRNK vaktsinalarining samaradorligini buzadi (Pang va boshq. 2022). Shunisi e'tiborga loyiqki, bir nechta tasdiqlangan nuklein kislota vaktsinalari (ZyCoV-D, intradermal tarzda qo'llaniladigan DNK plazmid vaktsinasi, Hindiston), BNT162b2 (mRNK, 2 doza, Germaniya), mRNK- 1273 (Moderna, AQSh, 2 doza), ARCoV (WALVAX, Xitoy) va klinik sinovlar, jumladan 302-COVID19 (DNK plazmid vaktsinasi, II/III mushak ichiga, Yaponiya), INO-4800 (DNK plazmid, II/III faza, intradermal, Xitoy), GX{{36} }}N (DNK vaktsinasi, Genexine, II/III faza), Covigenix VAX-001 (DNK vaktsinasi, Entos Pharmaceuticals, I/II faza, mushak ichiga), COVID-eVax (DNK vaktsinasi, I/II faza, mushak ichiga) , Rim) va bacTRL-Spike (DNK vaktsinasi, I faza, og'iz orqali, Symvivo) ishlab chiqilgan (Sheridan 2021; Liu va Ye 2022a). Bu vaksinalar gumoral va hujayra immunitetini kuchaytirgan, bundan tashqari GX-19N va AG0302- COVID-19. COVID{45}} nuklein kislotasiga asoslangan vaktsinalarning ayrim salbiy taʼsiri orasida ogʻriq, limfadenopatiya, eritema, qizarish, shishish, koʻngil aynishi, charchoq, artralgiya, miyalji, isitma, yurak-nafas olishni toʻxtatish, insult, yuqori sezuvchanlik reaktsiyasi, alkogolli jigar kasalligi, Bell kasalligi kiradi. , paroksismal qorincha aritmi va o'lim (Norquist va boshq. 2012; McNeil va DeStefano 2018; Baden va boshq. 2021; Momin va boshq. 2021; Liu va Ye 2022b, 2022a).
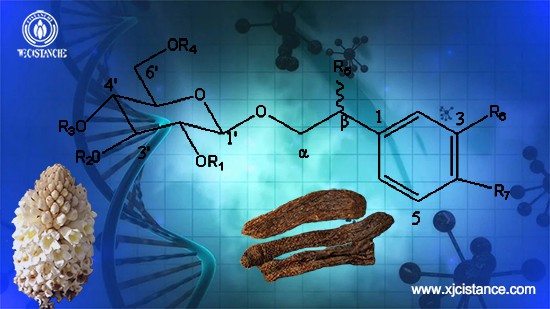
Feniletanol glikozid Cistanche deserticolaning asosiy faol komponentidir
Xulosa
Tezkor COVID-19 pandemiyasi kasallikning oldini olish uchun samarali vaktsinalarni ishlab chiqish zaruratini keltirib chiqardi. Hayvonlarda DNK vaktsinalarining immunogenligi maqbul bo'lsa-da, odamlarda klinik tekshirish kafolatlanadi. RNK vaktsinalari tegishli immunologik xususiyatlarni va DNK vaktsinalariga nisbatan katta afzalliklarni taqdim etishi mumkin. RNKning beqaror tabiati bilan bog'liq muammolar uning emirilishini to'xtatish uchun tegishli saqlash yondashuvlari va formulalari yordamida hal qilindi. Vaktsina xavfsizligi ham muhim va yuqori samaradorlik uchun buzilmasligi mumkin. COVID-19 tarqalishini nazorat qilish uchun tasdiqlangan nuklein kislotasi asosidagi vaktsinalar mavjud. Ishtirokchilarni kuzatish davom ettirilishi kerak. Nuklein kislotasi asosidagi COVID-19 vaksinasining nojo‘ya ta’sirini o‘rganish zarur. Bundan tashqari, vaktsinalarni qayta baholash va polivalent vaktsinalarni ishlab chiqish yoki pan-koronavirus strategiyalari tashvishli yangi variantlarning qayta paydo bo'lishini hisobga olgan holda istiqbolli.
1-jadval Klinik sinovlar va tasdiqlangan COVID{1}} vaksinalari va ularning xususiyatlari


Ma'lumotnomalar
Abdelmageed MI va boshqalar (2020) Inson COVIDning E oqsiliga qarshi multiepitopli peptidli vaktsinani loyihalash-19: immun informatika yondashuvi. Int J Biomed Clin Anal. https://doi.org/ 10.1155/2020/2683286
Abera G, Berhanu G, Tekewe A (2012) Ribozimlar: potentsial farmatsevtik dasturlarga ega nuklein kislota fermentlari: sharh. Farmakofora 3: 164–178
Ahn JY va boshqalar (2022) Spike yoki spike va nukleokapsid oqsillarini kodlash hududlarini o'z ichiga olgan ikkita rekombinant DNK COVID-19 vaktsinalarining xavfsizligi va immunogenligi: ikkita ochiq yorliqli, tasodifiy bo'lmagan, 1-bosqich sinovlarining oraliq tahlili sog'lom kattalarda. Lancet Microbe 3: e173–e183. https://doi.org/10.1016/ S2666-5247(21)00358-X
Aihara H (1998) Miyazaki J. genini in vivo elektroporatsiya orqali mushak ichiga o'tkazish. Nat Biotechnol 16:867–870. https://doi.org/10. 1038/nbt0998-867
Alberer M va boshqalar (2017) Sog'lom kattalardagi mRNK quturgan vaktsinasining xavfsizligi va immunogenligi: ochiq yorliqli, tasodifiy bo'lmagan, istiqbolli, insonda birinchi bosqich 1 klinik sinovi. Lancet 390: 1511-1520.https://doi.org/10.1016/s0140-6736(17)31665-3
Amante DH va boshqalar (2015) Teri transfektsiyasi naqshlari va CELLECTRA -3P, portativ yangi avlod dermal elektroporatsiya qurilmasi yordamida elektroporatsiya bilan kuchaytirilgan plazmid etkazib berishning ekspression kinetikasi. Inson gen terapiyasi usullari 26:134–146. https:// doi.org/10.1089/hgtb.2015.020
Anand P, Stahel VP (2021) Covid{1}} mRNK vaksinlarining xavfsizligini ko'rib chiqing: sharh. Bemor Saf Surg 15:20. https://doi.org/10.1186/ s13037-021-00291-9
Baden LR va boshqalar (2021) mRNK -1273 SARS CoV-2 vaktsinasining samaradorligi va xavfsizligi. N Engl J Med 384:403–416. https://doi.org/10. 1056/NEJMoa2035389
Becker PD, Noerder M, Guzman CA (2008) Genetik immunizatsiya: bakteriyalar DNK vaktsinasini etkazib berish vositalari sifatida. Hum vaktsinasi 4:189–202.https://doi.org/10.4161/hv.4.3.6314
Borah P va boshqalar (2021) COVID uchun RNK vaktsina nomzodlari boʻyicha istiqbollar-19. Old Mol Biosci. https://doi.org/10.3389/fmolb. 2021.635245
Brocato RL va boshqalar (2021) SARS-CoV-2 DNK vaktsinasining yovvoyi va immuniteti zaif suriyalik hamsterlarda himoya samaradorligi. Npj vaktsinalari 6:1–7.https://doi.org/10.1038/s41541-020-00279-z
Brüssow H (2020) COVID-19ga qarshi vaksinaga intilish. Environ Microbiol 22:4071–4084. https://doi.org/10.1111/1462-2920. 15225
Buchholz UJ va boshqalar (2004) Koronavirusning og'ir o'tkir respirator sindromi tarkibiy oqsillarining himoya immunitetiga qo'shgan hissasi. Proc Natl Acad Sci 101: 9804–9809. https://doi.org/ 10.1073/pnas.0403492101
Kempbell JD (2017) CpG adjuvanti 1018 ni ishlab chiqish: vaziyatni o'rganish. Adjuv vaktsina. https://doi.org/10.1007/ 978-1-4939-6445-1-2
Carter C va boshqalar (2019) Sog'lom kattalarda intradermal yoki mushak ichiga yuboriladigan uch valentli inaktivlangan vaktsinadan so'ng mavsumiy grippga qarshi gemagglutinin DNK vaktsinasining xavfsizligi va immunogenligi: ochiq yorliqli randomizatsiyalangan 1-bosqich klinik sinov. PLoS One 14: e0222178. https://doi.org/10.1371/ journal.pone.0222178
Chapin-Bardales J, Gee J, Myers T (2021) mRNKga asoslangan COVID{3}} vaktsinalarini olgandan keyin reaktogenlik. JAMA. https://doi. org/10.1001/jama.2021.5374
Chen Y, Cheng L, Lian R, Song Z, Tian J (2021) COVID{1}} vaktsinasi boʻyicha tadqiqotlar xavfsizlik, samaradorlik, immunoinformatika hamda vaksina ishlab chiqarish va yetkazib berishga qaratilgan: VOSviewer asosida bibliometrik tahlil. Biosci tendentsiyalari. https://doi.org/10.5582/bst.2021. 01061
Choi Y, Chang J (2013) Vaktsinalar uchun virusli vektorlar. Clin Exp Vaccine Res 2:97.https://doi.org/10.7774/cevr.2013.2.2.97
Chowdhury MA, Hossain N, Kashem MA, Shahid MA, Alam A (2020) COVIDdagi immunitet reaktsiyasi-19: Sharh. J Jamoat salomatligini yuqtirish. https://doi.org/10.1016/j.jiph.2020.07.001
Koban C, Kobiyama K, Jounai N, Tozuka M, Ishii KJ (2013) DNK vaksinlari: oddiy DNKni sezuvchi moddami? Hum Vaccin Immunother 9: 2216–2221.https://doi.org/10.4161/hv.25893
Conforti A va boshqalar (2022) SARS-CoV-2 RBD ni kodlovchi elektroporatsiyalangan DNK vaktsinasi nomzodi COVID-eVax hayvonlar modellarida himoya reaktsiyalarini keltirib chiqaradi. Mol Ther 30:311–326. https://doi. org/10.1016/j.ymthe.2021.09.011
Conforti A, Sanchez E, Salvatori E, Lione L, Compagnone M, Pinto E va boshqalar (2023) SARS CoV-2 retseptorlari bog‘lovchi domenini kodlovchi chiziqli DNK vaktsina nomzodi uy mushuklarida kuchli immun javob va neytrallovchi antikorlarni keltirib chiqaradi. Mol Ther-Metho Clinic Dev 28:238–248. https://doi.org/10.1016/j.omtm.2022. 12.015
Croyle M, Cheng X, Wilson J (2001) Gen terapiyasi uchun virusli vektorlarning jismoniy barqarorligini oshiradigan formulalarni ishlab chiqish. Gen Ther 8: 1281–1290.https://doi.org/10.1038/sj.gt.3301527
Cu Y va boshqalar (2013) In situ elektroporatsiya orqali o'z-o'zini kuchaytiruvchi mRNK vaktsinalarini etkazib berish va kuchayishi. Vaktsinalar 1:367–383. https://doi.org/10.3390/vaccines1030367






